- Las enfermedades parasitarias en los rumiantes afectan al estado sanitario y al bienestar animal, causando grandes pérdidas económicas. Además, algunas de ellas son importantes zoonosis. El control de una gran parte de las enfermedades parasitarias en los rumiantes está basado en su tratamiento farmacológico en combinación con diferentes medidas de bioseguridad y de manejo. Sin embargo, la aparición de estirpes de parásitos resistentes frente a determinados fármacos antiparasitarios, la presencia de residuos en los alimentos y en el ambiente o los vacíos terapéuticos, han determinado que la inmunoprofilaxis sea una alternativa necesaria. La vacunación puede evitar o atenuar las manifestaciones clínicas de las enfermedades y su transmisión, prevenir y controlar enfermedades zoonósicas, disminuir la necesidad de administrar un tratamiento farmacológico y aumentar la producción y el bienestar animal.
- A pesar de ello, aún existen muy pocas vacunas antiparasitarias comercializadas, debido a la elevada complejidad antigénica de los parásitos (diferentes estadios de los agentes parasitarios, variabilidad entre cepas o especies), de sus ciclos biológicos y de la respuesta inmunitaria de los rumiantes, dependiente de las variaciones fisiológicas o patológicas a lo largo de su vida y, en determinados casos, a un menor tamaño del mercado. El tiempo que trascurre desde el desarrollo de una nueva vacuna, su validación (seguridad y eficacia en las especies de destino) hasta la disponibilidad comercial, pueden ser de 10 años o más. Todo ello conlleva una menor inversión en su investigación y desarrollo.
En varias entregas de este blog se van a ir describiendo las principales vacunas antiparasitarias disponibles para su uso en rumiantes. En esta entrega se presentan las disponibles frente a enfermedades causadas por protistas (I). En posteriores contribuciones se irán presentando las disponibles frente a helmintos (II) y artrópodos (III). Esta serie monográfica concluirá con la presentación de los principales avances e investigaciones realizadas en el desarrollo de vacunas de nueva generación frente a parásitos (IV).
VACUNAS FRENTE A ENFERMEDADES CAUSADAS POR PROTISTAS
Las enfermedades causadas por este grupo de parásitos tienen una gran importancia clínica y productiva en los rumiantes domésticos pudiendo causar: fallo reproductivo (ej. toxoplasmosis, neosporosis, besnoitiosis y tricomonosis), fiebre, anemia, abortos y reducción de la producción de leche (ej. piroplasmosis), diarrea y pérdida de peso (ej. coccidiosis y criptosporidiosis) y en casos graves la muerte del animal. Además, algunos de estos parásitos que afectan a los rumiantes domésticos pueden también transmitirse a los humanos como Toxoplasma gondii y Cryptosporidium parvum. Actualmente, solo hay vacunas en el mercado disponibles en algunos países frente a la toxoplasmosis ovina, la tricomonosis bovina y las piroplasmosis en el ganado bovino. En países que no cuentan con registro o licencia de estas vacunas, pueden importarse previa aprobación de la agencia regulatoria en cada país. La mayoría de estas vacunas (excepto las vacunas frente a la tricomonosis) son vacunas vivas, capaces de inducir una respuesta inmunitaria de tipo celular muy semejante o igual a la que tendría lugar en una infección natural y que es clave para su control. Sin embargo, presentan importantes limitaciones desde el punto de vista de su seguridad, producción y distribución. Además, en los últimos años se está trabajando intensamente en el desarrollo de vacunas frente a otras parasitosis, como la neosporosis bovina o la criptosporidiosis. A continuación, se describen tanto las vacunas comerciales como las que se encuentran todavía en fase de desarrollo.
Toxoplasmosis ovina
- La toxoplasmosis, cuyo agente etiológico es T. gondii, es una de las causas transmisibles más importantes de fallo reproductivo en el ganado ovino y una de las principales zoonosis de transmisión alimentaria. Actualmente, existe una vacuna viva atenuada (Toxovax®) comercializada en Nueva Zelanda, Reino Unido, Irlanda, España, Francia y Noruega. El componente activo de esta vacuna es el estadio de taquizoíto de T. gondii de la cepa S48. El parásito se ha sometido a numerosos pases en ratón de laboratorio y, aparentemente, ha perdido la capacidad de diferenciarse a bradizoíto y de formar quistes tisulares (presentes en la fase crónica de la infección), por lo que supuestamente no persiste en los tejidos de la oveja.
- Toxovax® está indicada para reducir el aborto y la mortalidad perinatal de los corderos causados por la toxoplasmosis ovina. En los estudios realizados, la vacuna parece conferir una protección significativa frente al aborto después del desafío oral con ooquistes de T. gondii y protege frente a la transmisión congénita durante al menos 18 meses.
- La vacuna se administra por la vía intramuscular, al menos 3 semanas antes de la cubrición. Si se administra por primera vez en el rebaño, se recomienda vacunar todo el rebaño y después solamente a las corderas de reposición a partir de los 4-5 meses de edad. No se debe vacunar ovejas gestantes. Después de los 2 años habría que revacunar de nuevo a todas las reproductoras con una dosis única al menos 3 semanas antes de la cubrición.
- Toxovax® es una vacuna viva y presenta importantes limitaciones, como su posible reversión a la virulencia, el riesgo potencial de convertir en portadores a algunos de los animales vacunados o de infectar al personal que la administra, debiéndose evitar su manipulación por mujeres gestantes. Asimismo, también presenta limitaciones comerciales, ya que la vacuna se produce únicamente bajo demanda, se debe transportar en refrigeración y tiene una corta vida útil (7-10 días a 4°C). Por tanto, el desarrollo de vacunas inactivadas que eviten los problemas asociados a la vacuna viva actual es una necesidad.
- Por otra parte, una vacuna frente a la toxoplasmosis, además de mejorar la productividad de los rebaños ovinos al reducir (o prevenir) el daño fetal, también sería de utilidad para reducir la presencia de quistes tisulares en la musculatura de los animales, teniendo en cuenta el carácter zoonósico de esta parasitosis. En este sentido, recientemente, se ha descrito que esta vacuna reduce la carga parasitaria en los tejidos, pero no previene la formación de quistes tisulares siendo necesarios más estudios al respecto.
Tricomonosis bovina
- La tricomonosis bovina, también conocida como “catarro vaginal contagioso” o “peste de la cubrición”, está causada por Tritrichomonas foetus y es una enfermedad de transmisión sexual que ocasiona fallo reproductivo temprano en el ganado bovino y es frecuente en los sistemas de explotación extensivos donde se usa la monta natural, produciendo importantes pérdidas económicas. Las vacunas disponibles frente a la tricomonosisis bovina están comercializadas en los EE.UU. (TrichGuard®) y Argentina (Tricovac®). La vacunación es sólo eficaz en las vacas y novillas y, aunque no previene la infección, reduce su gravedad y sus efectos. De esta forma, el empleo de estas vacunas permite generar una respuesta inmunitaria que reduzca el tiempo de infección por T. foetus en las hembras vacunadas antes de que la misma sea un riesgo para el embrión/feto, disminuyendo las pérdidas económicas asociadas. Estas vacunas están elaboradas con trofozoítos del parásito inactivados mediante diferentes técnicas físico-químicas y se administran por vía parenteral una o dos veces al año antes de la cubrición.
- Recientemente se ha aprobado por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) la autorización de comercialización de una vacuna en España (Trichobovis®) desarrollada por el grupo SALUVET y la ETCU-UCM SALUVET-INNOVA S.L. que presenta una mayor eficacia que la vacuna comercializada en EE.UU. El uso de esta vacuna puede facilitar el control de la enfermedad en España en rebaños donde se utiliza la monta natural, ya que hoy en día la tasa de prevalencia de la tricomonosis en nuestro país es elevada. Además, su empleo en una explotación infectada permite mejorar los parámetros reproductivos asociados a esta enfermedad en los animales vacunados (Tabla 1). Por tanto, la vacunación podría ser una medida de control beneficiosa en rebaños expuestos a factores de riesgo, como el uso de pastos comunales, falta de pruebas diagnósticas y una elevada proporción de toros mayores de 3 años.
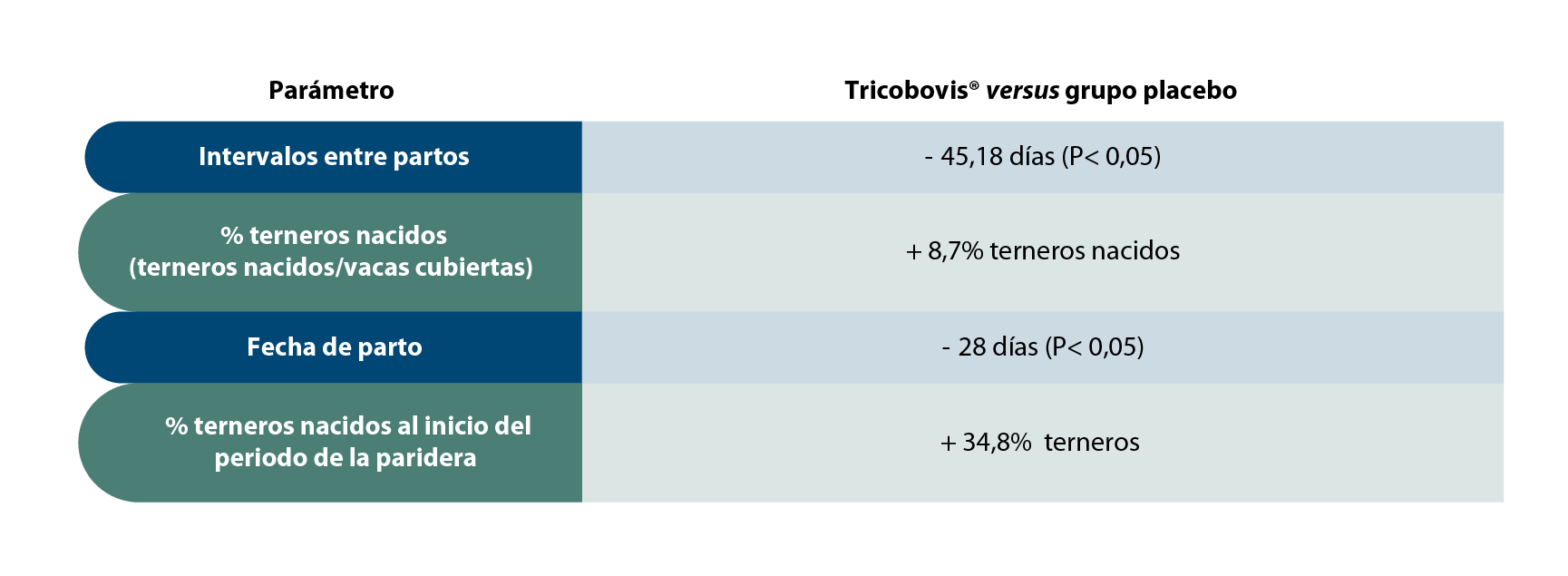
Tabla 1. Comparación de los datos reproductivos entre animales vacunados con la vacuna Trichobovis® y el grupo Placebo.
Babesiosis bovina
- La babesiosis bovina es una parasitosis hemática transmitida por ixódidos y producida por especies del género Babesia que cursa habitualmente con fiebre, anemia, hemoglobinuria, ictericia e incluso la muerte del animal. El desarrollo de vacunas frente a la babesiosis bovina fue impulsado por las observaciones que indicaban que las vacas infectadas se recuperaban y desarrollaban una inmunidad duradera y que los pases sanguíneos sucesivos del parásito entre terneros esplenectomizados ocasionaban una disminución progresiva en la virulencia del parásito. De esta forma, las vacunas actualmente disponibles están elaboradas con parásitos vivos, en los que los animales donantes (terneros esplecnetomizados) se inoculan con cepas atenuadas adecuadas, se les extrae sangre de la vena yugular durante la fase aguda de la infección y se determina la parasitemia con el fin de normalizar el número de eritrocitos infectados por dosis de vacuna. El control de calidad posterior a la producción comprende la esterilidad, la potencia (viabilidad de los organismos inmunizantes), la seguridad (grado de atenuación) y la eficacia (capacidad para proteger frente a un desafío con una cepa virulenta). Además, los bovinos donantes deben mantenerse libres de Babesia y otros patógenos y las vacunas deben someterse a estrictos controles de calidad para evitar la diseminación de otros patógenos en el momento de la vacunación. En algunos centros de producción de vacunas han adoptado algunas mejoras como una vida útil más prolongada mediante la ultracongelación o el cultivo de parásitos in vitro con el fin de evitar el riesgo de la contaminación y diseminación de otros agentes infecciosos presentes en los animales donantes.
- Actualmente, no existen vacunas disponibles en Europa, pero hay algunas comercializadas frente a B. bovis y B. bigemina en varios países de Sudámerica, Australia, Israel y Sudáfrica (Tabla 2). También se comercializa una fórmula trivalente con eritrocitos infectados con la rickettsia Anaplasma centrale y que ofrece protección cruzada frente a Anaplasma. La producción comercial de vacunas vivas frente a B. divergens se suspendió hace más de 10 años en Irlanda, y no hay información disponible sobre la producción actual en otros países. Las vacunas que están actualmente comercializadas no son producidas a gran escala, tienen distribución regional y se fabrican, principalmente, con apoyo gubernamental en los países donde está permitido su uso (Tabla 2).
- La vacunación está indicada en terneros de 4 a 10 meses. La inmunidad se desarrolla a las 3-4 semanas después de la vacunación y normalmente dura, al menos, 4 años, confiriendo una alta protección. Los animales adultos pueden desarrollar babesiosis aguda después de la vacunación, por lo que se recomienda un seguimiento diario de hasta 21 días. Se desaconseja la eliminación completa de las garrapatas después de la vacunación, ya que las infecciones naturales por medio de las picaduras de las garrapatas ayudarían a adquirir un estado de protección a largo plazo. Por otro lado, las vacunas vivas frente a B. bovis y B. bigemina dan lugar a animales portadores resistentes a estas enfermedades que pueden actuar como reservorios.
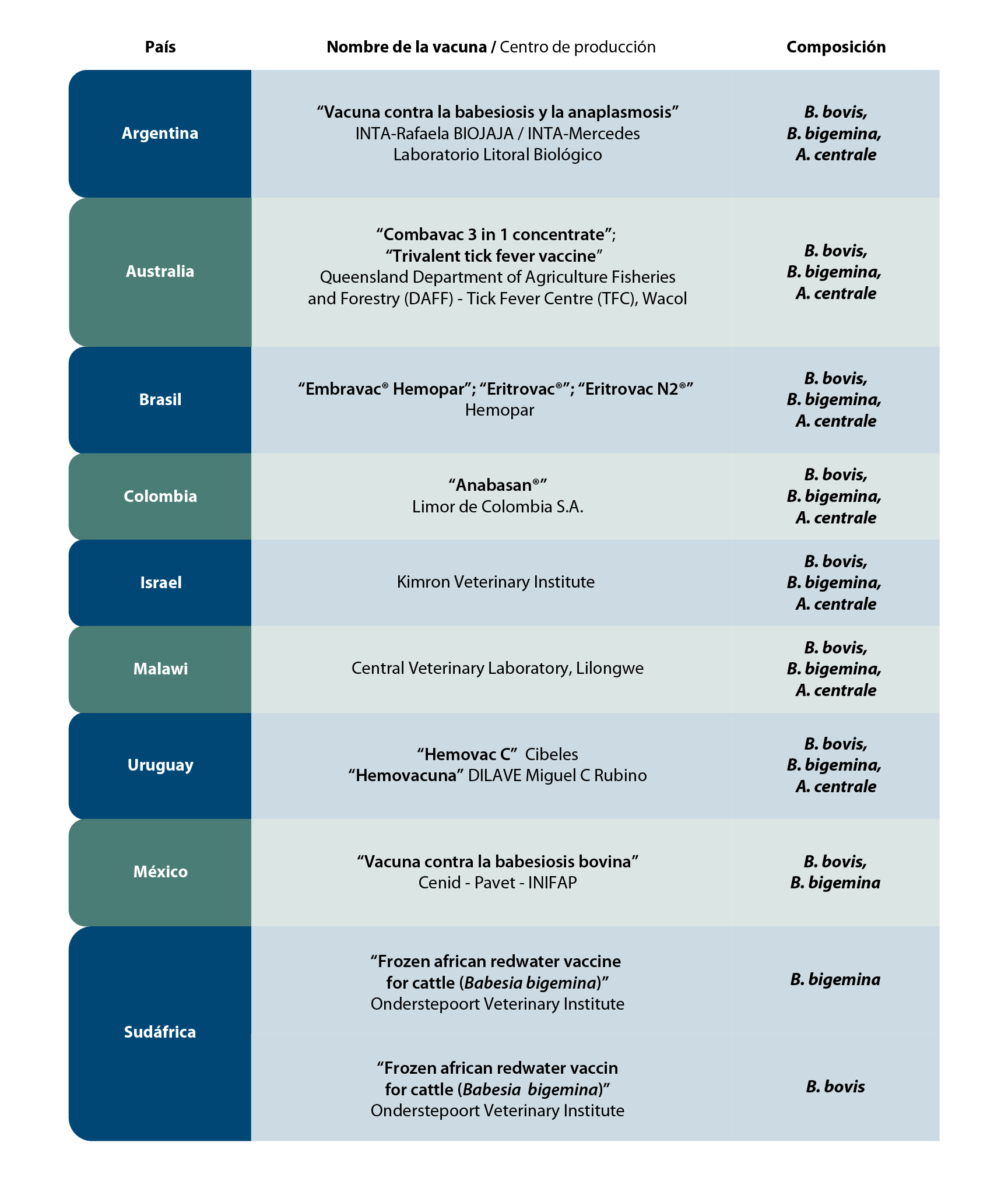
Tabla 2. Vacunas comercialmente disponibles frente a la babesiosis y anaplasmosis bovinas. A excepción de las vacunas del INTA-Rafaela y del Laboratorio Litoral Biológico (Argentina) que emplean eritrocitos infectados con B. bovis y B. bigemina producidos in vitro, el resto de las vacunas utilizan eritrocitos infectados obtenidos de terneros esplenectomizados.
Theileriosis bovina
– Fiebre de la costa mediterránea
- Theileria annulata es el agente causal de la theileriosis bovina en la cuenca mediterránea, también conocida como “Fiebre de la costa mediterránea” o “Theileriosis tropical”. Es una enfermedad parasitaria del ganado bovino, transmitida por garrapatas del género Hyalomma y que se caracteriza por ocasionar fiebre, linfadenomegalia, anemia, apatía y a veces mortalidad .
- Las vacunas desarrolladas frente a T. annulata son vacunas vivas atenuadas por cultivo del parásito en pases sucesivos en líneas celulares transformadas. La inmunización del ganado bovino con estas líneas celulares es capaz de inducir la infección del parásito en las propias células del hospedador, estimulando una respuesta inmunitaria protectora frente a los signos clínicos de la theileriosis.
- Las células infectadas con T. annulata pueden ser congeladas, permitiendo la preparación de un “stock master” que servirá para la realización de los cultivos necesarios para la preparación de las dosis de la vacuna. Sin embargo, su utilización implica pruebas con animales para comprobar la atenuación de la cepa vacunal (ausencia de fiebre y parásitos -esquizontes o piroplasmas- en terneros).
- Actualmente, no existen vacunas autorizadas frente la theileriosis bovina en Europa. Estas vacunas se producen localmente y se han usado en varios países como Israel, Irán, Marruecos, Túnez, India, China y Uzbekistán. Comercialmente, solo hay dos vacunas disponibles, una en Turquía y otra en India. La inmunización estaría recomendada en terneros mayores de 3 meses y en vacas con menos de 6 meses de gestación con una efectividad del 80%, tal y como se ha descrito en una estudios realizados con una vacuna elaborada en Túnez. Por su parte, la inmunidad inducida es de 14 meses hasta 4 años. Sin embargo, la eficacia y la duración de la inmunidad podría variar según la cepa vacunal empleada, la raza o edad del animal, las condiciones epidemiológicas de la zona, etc.
- Las vacunas vivas atenuadas actuales conllevan los inconvenientes asociados a las vacunas vivas (almacenamiento en nitrógeno líquido, estrictos controles de calidad), pero destacan los riesgos asociados a la introducción del genotipo de la cepa vacunal en la población de garrapatas autóctonas. Para solventar este problema se ha descrito que el parásito dentro de algunas líneas celulares pierde la capacidad de diferenciarse en merozoítos después de pases prolongados, lo que implicaría un menor riesgo de transmisión a las garrapatas. Otro inconveniente de estas vacunas es que se elaboran con aislados locales, por lo que no hay una vacuna comercializada universalmente o un método normalizado de producción. Además, el uso de estas vacunas no confiere una buena protección frente a otras cepas que pueden estar presentes en el mismo país, por lo que es necesario el desarrollo de otro tipo de vacunas con antígenos compartidos que induzcan una protección heteróloga. Por su parte, en alguna de las vacunas utilizadas en India y Rusia se ha descrito que pueden dar lugar a animales portadores, hecho relacionado con la falta de normalización y armonización en el desarrollo de estas vacunas (cepa vacunal utilizada, dosis de las células inyectadas, medios de cultivo, uso de células frescas o descongeladas) y su uso, ya que los niveles de atenuación varían con respecto a la raza y edades de los animales objeto de vacunación.
– Fiebre de la costa oriental
- Theileria parva es el causante de la “fiebre de la costa oriental”, una devastadora enfermedad del ganado bovino del África subsahariana. El parásito induce un síndrome linfoproliferativo que resulta en una muerte rápida en los animales susceptibles, particularmente en el ganado Bos taurus, pero también causa una alta mortalidad en el ganado cebú (Bos indicus) joven en los sistemas en pastoreo. En 1970 se desarrolló una estrategia de vacunación que consistía en la infección de bovinos con dosis definidas de esporozoítos criopreservados y la administración simultánea de una tetraciclina de acción prolongada. La administración del fármaco en el momento de la infección enlentece el desarrollo del parásito en el hospedador, dando tiempo al desarrollo de una respuesta inmunitaria específica que es capaz de controlar la infección. Los esporozoítos se obtienen de garrapatas infectadas y se prueba su potencia por titulación en bovinos. Este sistema de vacunación basado en el método de infección-tratamiento ha sido registrado recientemente en África por GALVmed financiada por la Fundación Bill y Melinda Gates (Figura 1).
- Se han realizado diversos ensayos de inmunización utilizando este método de vacunación en Zambia, Zimbabue y en pequeños sectores lácteos en Uganda y Tanzania. El programa de inmunización más extenso hasta la fecha, se llevó a cabo por una empresa privada (VetAgro) en Tanzania, donde se vacunó con éxito a más de medio millón de cabezas de ganado Massai y se observó una reducción del 95% de la mortalidad.
- A pesar de la efectividad de esta vacuna para inducir protección, su uso es limitado debido a problemas técnicos, éticos y políticos. Destaca la complejidad y variabilidad de la producción de los lotes, que incluyen la necesidad de pruebas extensas in vivo en el ganado bovino y el uso generalizado de oxitetraciclina en el campo. La producción y las pruebas de laboratorio de un lote de la vacuna viva para la inmunización de un millón de bovinos requiere ~130 bovinos y 500 conejos. Además, es necesaria la aplicación de al menos 600.000 garrapatas ninfas al ganado infectado para proporcionar suficientes garrapatas infectadas para controlar los niveles de infección y estabilizar la producción. Por otro lado, este sistema de vacunación puede dar lugar a animales portadores con una infección persistente y potencialmente transmisible por garrapatas, creando un escenario en el que las cepas vacunales, o alelos específicos dentro de las mismas, podrían recombinarse con las poblaciones de parásitos residentes, modificándose la dinámica de transmisión y la genética de la población de parásitos. Asimismo, como todas las vacunas vivas se requiere una cadena de frío para su distribución, ya que los esporozoítos deben administrarse rápidamente después de la descongelación de nitrógeno líquido. Todo ello ha limitado su uso.
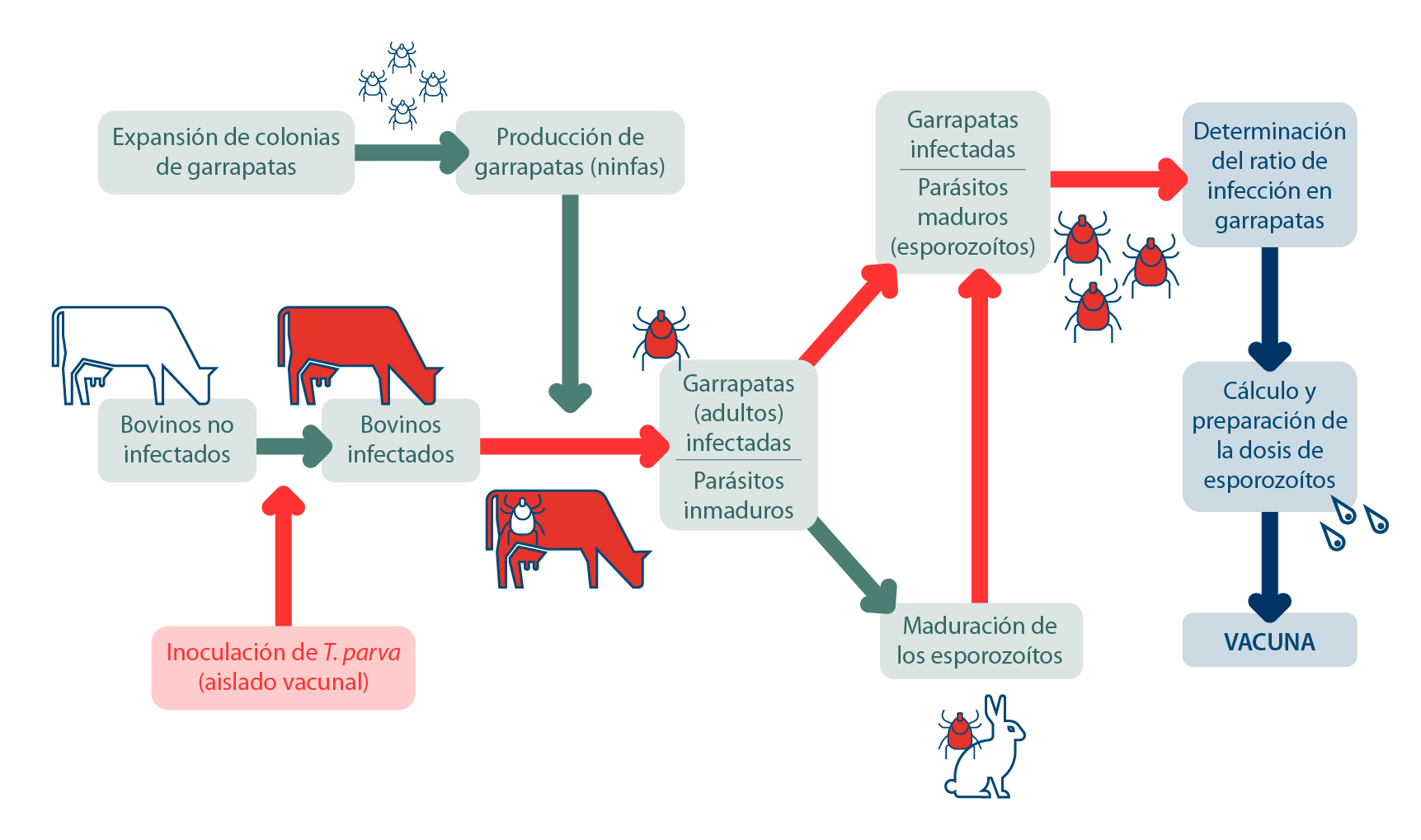
Figura 1. Diagrama de flujo que resume los procedimientos realizados en la producción de una vacuna de esporozoítos de T. parva. Las garrapatas ninfas no infectadas se alimentan sobre los bovinos infectados previamente con T. parva que mudarán hasta el estadio de adulto. A continuación, se induce la maduración de los esporozoítos en las garrapatas adultas infectadas que se alimentan en conejos. Para la producción de la vacuna se trituran las garrapatas infectadas y se calcula el ratio de garrapatas infectadas y la dosis de esporozoítos, según el análisis por microscopía realizado en las glándulas salivales diseccionadas. Posteriormente, la viabilidad se evalúa mediante infección y titulación in vitro e in vivo para determinar la dilución apropiada de la vacuna de esporozoítos frente a una dosis fija de oxitetraciclina.
Besnoitiosis bovina
- La besnoitiosis es una enfermedad del ganado bovino caracterizada por signos clínicos sistémicos inespecíficos y lesiones en la piel cuyo agente etiológico es Besnoitia besnoiti .
- Se han desarrollado algunas vacunas vivas que contienen parásitos atenuados en cultivo celular pero su uso no está regulado en Europa. En Sudáfrica, la vacuna se basa en taquizoítos de un aislado obtenido en un ñu y cultivado in vitro, recomendándose su uso en animales destetados y de mayor edad. Su aplicación protege al ganado frente a la besnoitiosis clínica, aunque no previene por completo de la infección subclínica. En Israel, se utiliza de forma habitual a todos los sementales importados. Se trata de una inoculación subcutánea de un aislado atenuado procedente de un toro infectado naturalmente. Sin embargo, no se ha realizado aún ningún estudio de eficacia y se desconoce su seguridad.
- Como ya se ha mencionado anteriormente, las vacunas vivas atenuadas presentan riesgos al introducir la cepa vacunal en rebaños no infectados y dar lugar a portadores entre los animales vacunados. Esto es especialmente preocupante en el caso de B. besnoiti, ya que el conocimiento sobre la biología, transmisión y ciclo biológico del parásito es todavía escaso.
Neosporosis bovina
- La neosporosis bovina, causada por Neospora caninum es una de las principales causas de aborto en el ganado bovino en todo el mundo. En la actualidad no existe ninguna vacuna en el mercado frente a la neosporosis bovina y sólo una vacuna inactivada (NeoGuard®) estuvo aprobada para su uso en vacas gestantes en los UU. hasta el año 2009. A pesar de ser una vacuna segura, su papel protector frente al aborto fue muy discutido, ya que no confería protección en vacas gestantes infectadas experimentalmente con el parásito y en varios estudios de campo presentó una eficacia variable (5,2%-54%).
- Hasta la fecha, los resultados más prometedores de protección frente al aborto se han obtenido tras el empleo de vacunas vivas atenuadas en infecciones experimentales en el ganado bovino. Sin embargo, las pruebas de seguridad asociadas a las vacunas vivas, su vida útil limitada y un alto coste de producción han impedido su comercialización, por lo que son necesarios nuevos estudios. El desarrollo de vacunas muertas que incluyan proteínas del parásito claves en su desarrollo así como diversas estrategias de vacunación (incluida la selección del adyuvante apropiado) deben estudiarse en detalle. Asimismo, es necesario el refinamiento de modelos apropiados de animales de experimentación y de infección.
Criptosporidiosis
- La criptosporidiosis es la principal causa de diarrea en terneros, corderos y cabritos de menos de un mes de vida y una zoonosis parasitaria, siendo Cryptosporidium parvum la especie más importante.
- La inmunización pasiva mediante la vacunación de las madres unas semanas antes del parto tiene como objetivo generar un calostro con altos títulos de anticuerpos específicos y se ha propuesto como una estrategia frente al control de la criptosporidiosis en los rumiantes. En paralelo, se reduciría la eliminación de ooquistes y la contaminación ambiental y la trasmisión de la infección a los rumiantes y a las personas. Recientemente, se ha patentado una vacuna recombinante con la proteína gp40 del parásito combinada con aziridina, si bien no se ha comercializado aún. Los terneros inmunizados con esta vacuna vía calostro mostraron una reducción en los signos clínicos asociados a la infección, como la diarrea.
- En el desarrollo de una vacuna frente a la criptosporidiosis sería necesario: i) identificar los componentes inmunitarios (tanto anticuerpos como factores inmunitarios celulares) del calostro que están asociados a la protección y la posterior transferencia de estos componentes a los neonatos; ii) estudiar el efecto de antígenos específicos del parásito que están involucrados en la estimulación de los componentes de la respuesta inmunitaria de la madre que pueden ser transferidos en el calostro; y iii) el desarrollo de un modelo in vivo que permita la evaluación de la seguridad y eficacia de una vacuna de calostro.
Los datos específicos sobre las vacunas descritas en este artículo se han obtenido de publicaciones o prospectos de las casas comerciales. Para consultar la bibliografía recomendada contactar con saluvet@ucm.es.

