Descripción: La sarcocistiosis bovina es una protozoosis sistémica de distribución mundial. Se caracteriza por la formación de quistes tisulares en la musculatura y está causada por alguna de las ocho especies descritas del género Sarcocystis que infectan específicamente al ganado vacuno. Las manifestaciones clínicas dependen de la especie parásita, del modo de transmisión y del estado inmunitario-fisiológico del hospedador.
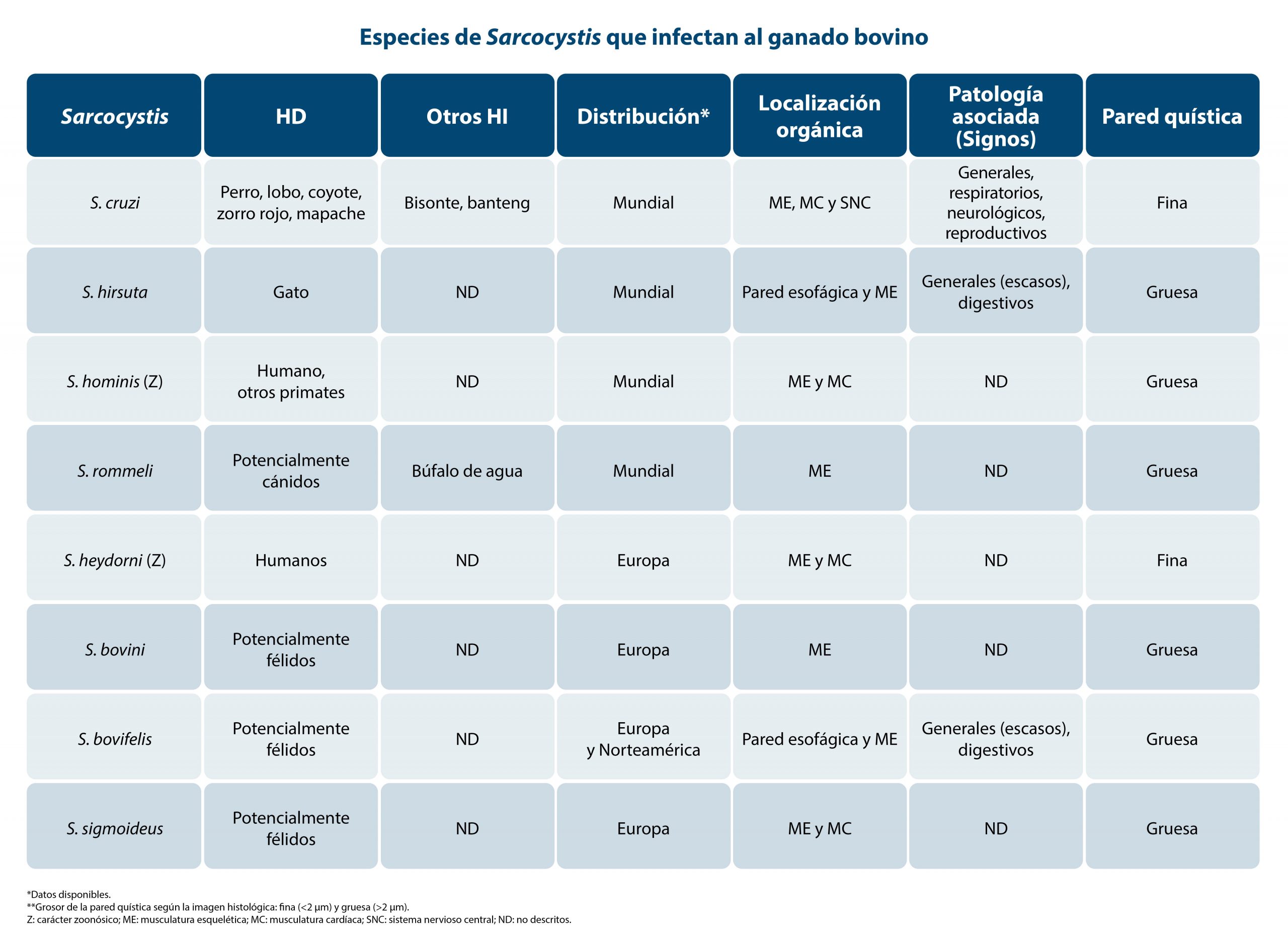
Etiología: Las Sarcocystis spp. (Phylum Alveolata, Fam. Sarcocystidae) son parásitos apicomplejos formadores de quistes tisulares, de las que Sarcocystis cruzi se considera la especie tipo (Tabla 1). En animales adultos la prevalencia individual está próxima al 80% debido al efecto acumulativo con la edad. La mayoría de las especies forman quistes microscópicos que no son detectados en la inspección sanitaria veterinaria post mortem, no así los formados por Sarcocystis hirsuta que pueden observarse en el tejido muscular justificando su decomiso. Además, Sarcocystis hominis tiene carácter zoonósico y junto con Sarcocystis bovifelis se consideran las principales responsables de la “miositis eosinofílica bovina” objeto de decomiso en mataderos.
Tabla 1. Especies de Sarcocystis que infectan al ganado bovino.
Zoonosis: Sí, es una zoonosis de transmisión alimentaria que se adquiere por la ingestión de carne cruda o poco cocinada de ganado vacuno. Existen dos especies, S. hominis y Sarcocystis heydorni, que tienen al ser humano como hospedador definitivo (HD) y en el que desarrollan la fase intestinal de su ciclo biológico, pudiendo causar la aparición de síntomas gastrointestinales (diarrea, dolor abdominal y vómitos).
¿Cuál es el ciclo biológico de Sarcocystis?
- El género Sarcocystis es extremadamente diverso en cuanto al número de especies que incluye. Actualmente se han descrito hasta 200 especies que parasitan a mamíferos, aves y reptiles; y que presentan un alto grado de especificidad por su hospedador intermediario (HI). Por ello y a modo de ejemplo, las especies que parasitan a los pequeños rumiantes no parasitan a los bóvidos y viceversa. El ganado vacuno actúa como HI para 8 especies (Tabla 1).
- El ciclo biológico de las Sarcocystis spp. es heteroxeno obligado y la transmisión es mediante carnivorismo en el HD (Figura 1).
- Los HD son félidos, cánidos y humanos en los que se produce la reproducción sexual del parásito en el intestino delgado (Figura 1: ciclo entero-epitelial). Los ooquistes esporulan en la luz intestinal (esporogonia) formándose en su interior dos esporoquistes con cuatro esporozoítos (estadio infectante) cada uno. Los HD eliminan en sus heces los esporoquistes (fase de resistencia del parásito durante algunas semanas en el ambiente) al producirse la ruptura de la pared de los ooquistes en la luz intestinal. La eliminación (periodo de patencia) dura varias semanas o meses porque los ooquistes quedan embebidos en la lámina propia del intestino delgado.
- En el ganado vacuno, que actúa como HI, tiene lugar la reproducción asexual del parásito, en la que se diferencian dos estadios, ambos infectantes (Figura 1: ciclo tisular o extra-intestinal):
-
- Merozoíto: estadio de multiplicación rápida del parásito que se produce en dos ciclos (merogonias) en diversos órganos, principalmente en los endotelios vasculares (especialmente en el hígado) y se asocia a la fase aguda de la infección
- Bradizoíto: estadio de multiplicación lenta asociado a la fase crónica de la infección. Cuando los merozoítos alcanzan su localización definitiva en la musculatura estriada (esquelética y cardíaca) y sistema nervioso central, se inicia el desarrollo de la vacuola parasitófora; y éstos se convierten inicialmente en metrocitos (redondeados) y posteriormente en bradizoítos (semilunares) que se localizan en el interior de quistes tisulares. El desarrollo de la pared quística es complejo y presenta una morfología particular con valor taxonómico.
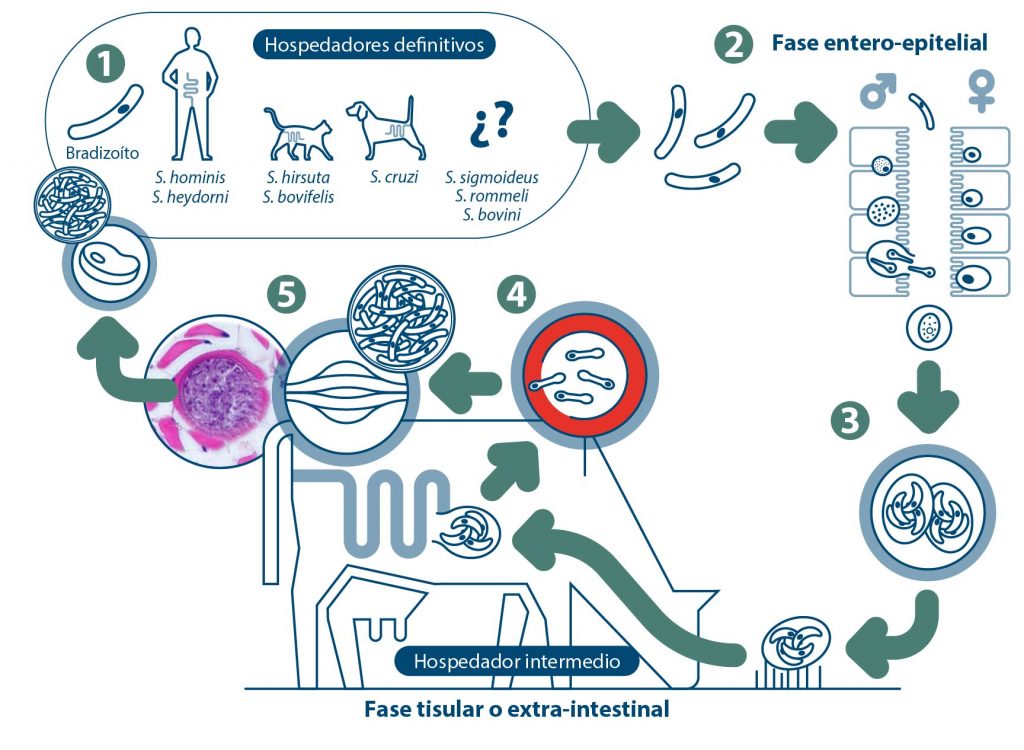
Figura 1. Ciclo biológico del género Sarcocystis. Los hospedadores definitivos (HD) específicos de cada especie de Sarcocystis se infectan principalmente al ingerir quistes con bradizoítos presentes en los tejidos del HI (carnivorismo) (1). En el intestino delgado se desarrolla el ciclo entero-epitelial (2): los bradizoítos se liberan durante la digestión y en las células de la mucosa intestinal se produce la gametogonia o reproducción sexual formándose el gameto femenino y masculino. Tras la fecundación se forma el cigoto que da lugar al ooquiste, el cual esporula en la luz intestinal (esporogonia) y queda embebido en la lámina propia; y seguidamente se produce la ruptura de la pared del ooquiste y se eliminan los esporoquistes con las heces (3). Cada ooquiste esporulado contiene dos esporoquistes, cada uno de los cuales contiene cuatro esporozoítos infectantes. Los HI se infectan al ingerir alimentos o agua contaminados con los esporoquistes (ruta fecal-oral) (4). En el aparato digestivo de los HI se liberan los esporozoítos, que penetran en la mucosa intestinal y pasan a la fase de merozoíto, desarrollándose el ciclo tisular u extra-intestinal. El merozoíto se asocia con la fase aguda de la infección, donde el parásito se distribuye y se multiplica asexualmente en dos ciclos por endopoligenia en el interior del citoplasma de las células endoteliales, inicialmente de los linfonodos mesentéricos y posteriormente, tras diseminación vía hemática, en diferentes órganos como hígado, bazo y riñón dependiendo de la especie parásita (ciclo lítico), dando lugar a numerosos merozoítos que egresan de la célula hospedadora, que tras lisarla, invaden otras nuevas. Como mecanismo de evasión de la respuesta inmunitaria del hospedador, la infección se cronifica y los merozoítos se convierten metrocitos y posteriormente en bradizoítos que se multiplican lentamente dando lugar a los quistes tisulares (5), que se localizan principalmente en el sistema nervioso central y en la musculatura estriada esquelética y cardíaca, permaneciendo viables durante la vida del hospedador.
¿Cómo se infectan los bovinos?
- Los HD se infectan al ingerir quistes tisulares del HI (carnivorismo o carroñerismo) que se encuentran principalmente en la musculatura esquelética, cardíaca y sistema nervioso central.
- El ganado vacuno se infecta por la ingestión de esporoquistes presentes en el agua de bebida, pasto, forraje o pienso. En el caso de rebaños en pastoreo, se observa un incremento de los animales infectados con la edad, ya que la respuesta inmunitaria que se instaura tras la primoinfección evita posteriores episodios clínicos, pero no impide la reinfección y la formación de nuevos quistes tisulares con efecto acumulativo.
- Aunque algunas especies de Sarcocystis (como S. cruzi) pueden causar abortos en vacas gestantes no se produce la infección congénita (ausencia de transmisión vertical).
¿Cuál es la patogenia, signos clínicos y lesiones asociados a la sarcocistiosis bovina?
- Debido a la diversidad de especies y a la escasez de datos contrastados sobre el carácter patógeno de algunas de ellas, se toma como especie tipo a S. cruzi, de la que existen diversos trabajos que incluyen infecciones experimentales. Existe un consenso en que S. cruzi es la especie más patógena y la más prevalente ya sea en infecciones únicas o mixtas con otras especies.
- Una vez ingeridos, los esporoquistes se desenquistan en el intestino delgado, liberándose los esporozoítos que invaden y se multiplican en las células del intestino y se diferencian en merozoítos, que por vía linfo-hematógena alcanzan los órganos diana, como el hígado, o invaden los endotelios vasculares donde se multiplican y causan daño tisular.
- La proliferación, mediante endopoligenia, de los merozoítos en los endotelios vasculares puede dar lugar a una reacción celular con la producción de linfocinas asociadas a fiebre, hipersensibilidad y aumento de la permeabilidad capilar y consecuente hemorragia. Por otro lado, se produce daño endotelial con la consiguiente activación de la cascada de la coagulación y aparición de trombos, con vasculitis y aparición de edemas, e inducción de cambios adicionales en la permeabilidad, responsable de las hemorragias asociadas.
- Con el desarrollo de la respuesta inmunitaria en el hospedador, los merozoítos se transforman en bradizoítos, inicialmente dentro de la vacuola parasitófora y, posteriormente, en el interior de quistes tisulares localizados principalmente en órganos inmunoprivilegiados, como el sistema nervioso central y la musculatura estriada. El animal permanecerá infectado de por vida y puede reinfectarse. Son comunes las infecciones mixtas por distintas especies de Sarcocystis, dando lugar a cargas parasitarias muy altas y fácilmente detectables por métodos diagnósticos directos.
- La sarcocistiosis es generalmente asintomática, aunque puede observarse un cuadro febril, anorexia, anemia, pérdida de peso, alopecia, debilidad, postración, hipersalivación, disminución de la producción de leche y muerte, entre otros signos, cuya gravedad dependerá de la dosis infectante de esporoquistes.
- Hasta el momento no se ha descrito la sarcocistiosis congénita, pero si se han descrito numerosos episodios de fallo reproductivo (como abortos) presumiblemente debido a los picos febriles que tienen lugar. El impacto de los abortos por las Sarcocystis spp. no ha sido apropiadamente evaluado hasta el momento.
- Se han descrito signos neurológicos en cuyo diagnóstico diferencial debería incluirse el parásito apicomplejo Neospora caninum.
- Existe un mecanismo patogénico particular conocido como miositis eosinofílica bovina que consiste en un proceso inflamatorio con causa incierta que se localiza usualmente en la musculatura de los miembros anteriores y posteriores. Algunos autores mencionan el carácter iatrogénico-traumático como consecuencia de la inyección de fármacos o bien la ruptura de la pared quística y exposición de los zoítos (bradizoítos) al sistema inmunitario ya inmunizado con la consecuente reacción celular (principalmente eosinófilos). Etiológicamente se ha observado un mayor grado de asociación de dos especies. S. hominis y S. bovifelis, con las lesiones y que, por tanto, podrían ser desencadenantes del proceso, si bien otras especies también se han encontrado asociadas a la lesión (como S. cruzi). Diversos estudios experimentales basados en la inoculación intramuscular de zoítos de diversas especies no lograron replicar las lesiones observadas en casos naturales.
¿Cómo saber si la sarcocistiosis está presente en mi granja?
- Debido a la inespecificidad de los signos clínicos y a la ubicuidad del género, el diagnóstico clínico-epidemiológico resulta de escasa utilidad.
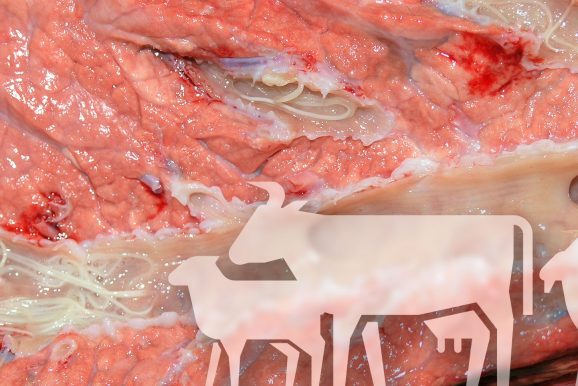
- El diagnóstico post-mortem (incluyendo la inspección en matadero) presenta limitaciones, ya que sólo permite la visualización de quistes macroscópicos de aproximadamente 1 cm, relacionados con S. hirsuta (Figura 2A) o de lesiones compatibles con miositis eosinofílica que conllevan el decomiso total o parcial de la pieza.
- Para detectar la presencia de infección por Sarcocystis en una explotación es necesaria la confirmación laboratorial.
- Las pruebas serológicas (ej. ELISA) para detectar anticuerpos específicos son poco informativas y quizás sólo interesantes para identificar el grado de seroconversión. La determinación de IgE podría ser una herramienta de interés. La presencia de reacciones cruzadas entre especies de Sarcocystis y otros parásitos apicomplejos es un aspecto importante a tener en cuenta.
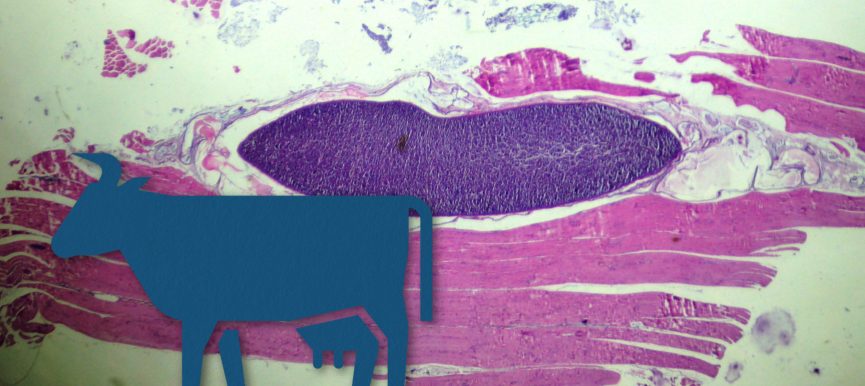
- Puesto que la mayor parte de las especies de Sarcocystis dan lugar a quistes tisulares microscópicos, resultan muy informativos los exámenes con microscopía óptica, bien mediante compresión en placa de triquineloscopía (Figura 2C) de porciones de musculatura o mediante histología (Figura 2D) que permite medir el grosor de la pared y observar la presencia de vellosidades y septos que confirman la identidad de los quistes como pertenecientes al género Sarcocystis. En casos agudos, la presencia de esquizontes (rosetas de merozoítos) puede observarse especialmente en tejido nervioso.
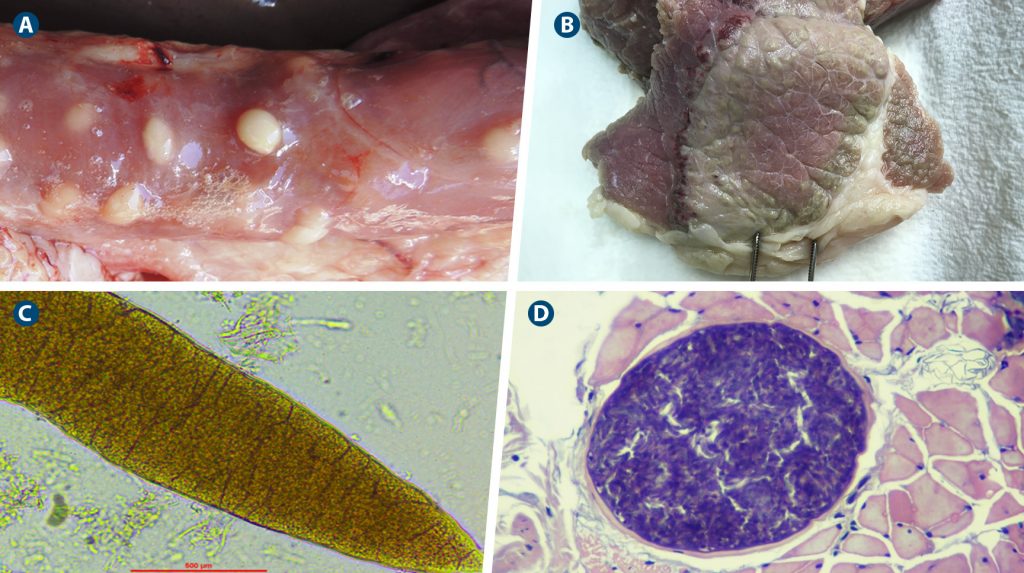
Figura 2. Lesiones macro (A, B) y microscópicas (C, D) de la infección por Sarcocystis spp. en ganado vacuno. A. Quistes de Sarcocystis hirsuta. B. Lesión verdosa de miositis eosinofílica bovina. C. Imagen microscópica de quiste de Sarcocystis spp. mediante compresión de tejido fresco en placa de triquineloscopía. D. Imagen microscópica de S. cruzi (Hematoxilina-eosina).
¿Cómo se puede controlar y prevenir la sarcocistiosis?
- No existe ningún fármaco autorizado para el control terapéutico o metafiláctico de la sarcocistiosis.
- No existen vacunas disponibles.
- Una estrategia de control podría ser mantener los animales seropositivos, ya que no van a sufrir episodios clínicos posteriores.
- Es importante reforzar las medidas higiénico-sanitarias y de bioseguridad encaminadas a reducir la contaminación ambiental y la transmisión (Figura 3):
- Controlar la población de gatos y perros en la explotación. Considerar también en la medida de lo posible controlar el acceso de otros carnívoros salvajes, como zorros o mustélidos que también actúan como HD (ej. S. cruzi).
- Impedir el acceso de potenciales HD a las zonas de almacenamiento de alimento y agua.
- Evitar alimentar carnívoros con despojos animales.
- Evitar el consumo de carnes poco cocinadas
- Adecuada depuración de aguas residuales y evitar el acceso de los animales a heces humanas.

Figura 3. Medidas profilácticas frente a la sarcocistiosis. (A) Almacenamiento adecuado de alimentos. (B) Evitar alimentar a perros y gatos con despojos.