La toxoplasmosis es una parasitosis de distribución mundial cuyas manifestaciones clínicas dependen de la especie animal, modo de transmisión y del estado inmunitario del hospedador. El agente etiológico es un parásito apicomplejo formador de quistes, Toxoplasma gondii (Phylum Alveolata, Familia Sarcocystidae). En los pequeños rumiantes, la toxoplasmosis es una de las causas transmisibles más importantes de fallo reproductivo, produciendo graves pérdidas económicas para los productores de este sector. Se estima que esta enfermedad es la responsable del 10-23% de los abortos ovinos en Europa y EE.UU. En cambio, la infección por T. gondii en el ganado bovino no es una causa relevante de fallo reproductivo.
Zoonosis: Sí. La toxoplasmosis es una de las principales zoonosis de transmisión alimentaria (ver capítulo de zoonosis).
Hospedadores, estadios parasitarios, ciclo biológico y transmisión
- Toxoplasma gondii presenta un ciclo biológico heteroxeno (Figura 1). Los hospedadores definitivos (HD) son los gatos y otros félidos, en los cuales se produce la reproducción sexual del parásito en el intestino. Los HD eliminan los ooquistes(fase de resistencia del parásito) con sus heces. Los ooquistes esporulan en el ambiente (esporogonia) formándose en su interior dos esporoquistes con cuatro esporozoítos (estadio infectante).
- Los hospedadores intermediarios (HI) son la mayoría de los animales homeotermos como las aves, mamíferos acuáticos y terrestres, incluyendo al gato, el cual puede actuar como HD y HI. En el HI tiene lugar la reproducción asexual del parásito y se diferencian dos estadios parasitarios (Figura 1: ciclo tisular), ambos infectantes:
- Taquizoíto: estadio de multiplicación rápida del parásito. Se localiza en una gran variedad de tipos celulares y está presente durante la fase aguda de la infección, siendo el responsable de la transmisión transplacentaria.
- Bradizoíto: estadio de multiplicación lenta asociado a la fase crónica de la infección. Se localiza en el interior de quistes tisulares rodeados por una pared, los cuales se encuentran principalmente en el sistema nervioso central y en la musculatura esquelética.
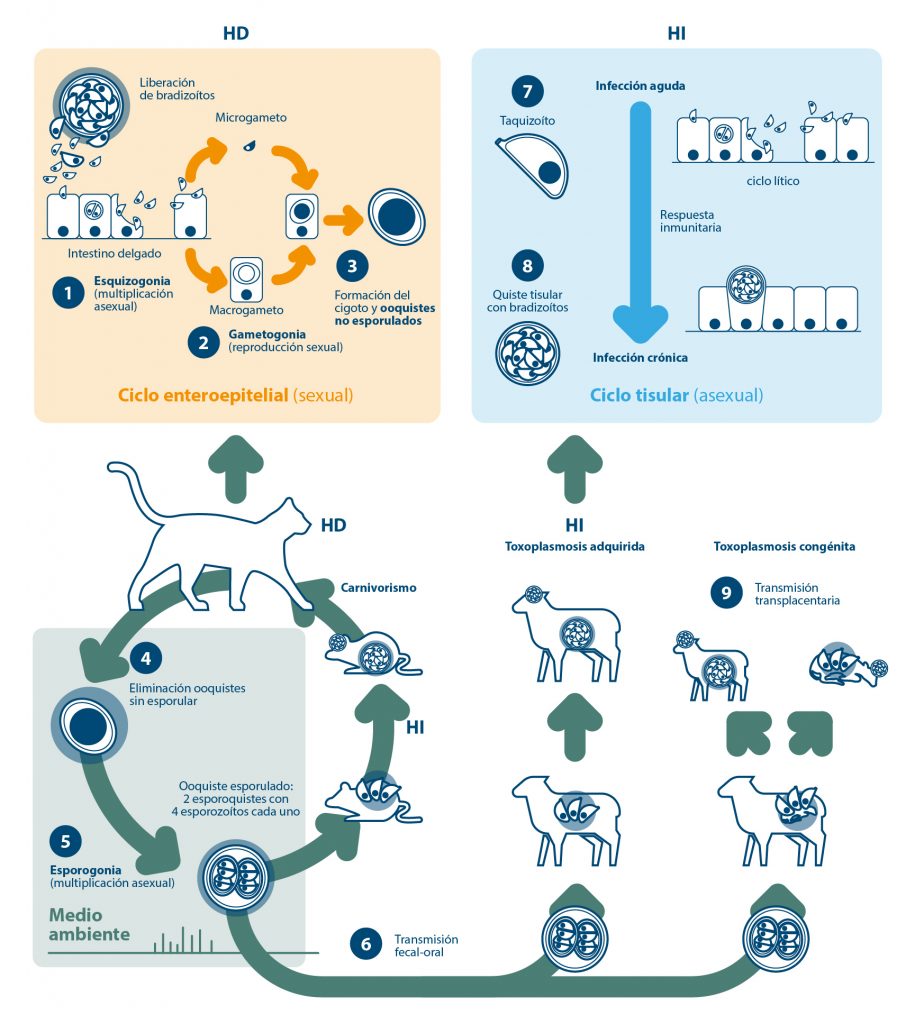
Figura 1. Ciclo biológico de Toxoplasma gondii. El gato (HD) se infecta principalmente al ingerir quistes con bradizoítos presentes en el HI (carnivorismo), aunque también podría infectarse por el consumo de ooquistes esporulados. En el intestino delgado se desarrolla el ciclo enteroepitelial: los bradizoítos o esporozoítos se liberan y en las células de la mucosa intestinal se produce la esquizogonia (1). Después de varias generaciones, tiene lugar la gametogonia o reproducción sexual (2) formándose el gameto femenino y masculino. Tras la fecundación se forma el cigoto que da lugar al ooquiste (3), el cual se elimina de forma no esporulada con las heces (4). En el ambiente tiene lugar la esporulación del ooquiste o esporogonia (5). Los ooquistes de T. gondii no son infectantes en el momento de la excreción y necesitan 3-5 días en el ambiente para ser infectantes. El ooquiste esporulado infectante contiene dos esporoquistes, cada uno de las cuales contiene cuatro esporozoítos infectantes. Los ooquistes se transmiten directamente al HI por la ruta fecal-oral (6). Los HI se infectan al ingerir alimentos o agua contaminados con ooquistes, o también por carnivorismo o carroñerismo, al ingerir quistes tisulares presentes en los tejidos de animales infectados. En el aparato digestivo de los HI se liberan los esporozoítos o bradizoítos, que penetran en la mucosa intestinal y se transforman en taquizoítos desarrollándose el ciclo tisular. El taquizoíto es el responsable de la fase aguda de la infección, donde el parásito se distribuye y se multiplica asexualmente por endodiogenia en el interior del citoplasma de las células de diferentes órganos (ciclo lítico), dando lugar a numerosos taquizoítos (7) que egresan de la célula hospedadora tras lisarla e invaden otras nuevas. Como mecanismo de evasión de la respuesta inmunitaria del hospedador, la infección se cronifica y los taquizoítos se convierten en bradizoítos que se multiplican lentamente dando lugar a los quistes tisulares, que se localizan principalmente en el sistema nervioso central y en la musculatura (8). Si el animal está gestante, los taquizoítos pueden atravesar la barrera placentaria durante la fase aguda del proceso y el parásito se transmite al feto por vía transplacentaria (toxoplasmosis congénita), pudiendo ocasionar su muerte o el nacimiento de animales congénitamente infectados (9).
- En relación con la transmisión del parásito, el gato se infecta al ingerir quistes tisulares del HI (carnivorismo o carroñerismo: ratones, pájaros, fetos abortados), aunque también podría infectarse al ingerir ooquistes esporulados. La mayoría de los gatos son resistentes a las reinfecciones y eliminan ooquistes una sola vez en su vida cuando se infectan por primera vez, normalmente cuando son jóvenes.
- El ganado ovino y caprino se infecta por la ingestión de ooquistes esporulados presentes en el agua de bebida, pasto, forraje o pienso (toxoplasmosis adquirida). En el caso de rebaños en pastoreo, la mayor parte de las ovejas tienen una seropositividad alta y se observa un incremento de animales seropositivos con la edad, ya que han tenido más posibilidades de exponerse al parásito a lo largo de su vida.
- Cuando el animal gestante se infecta, el parásito se transmite al feto tras cruzar la placenta (toxoplasmosis congénita), pudiendo ocasionar su muerte. Un gato puede expulsar en sus heces más de 500 millones de ooquistes, cantidad muy elevada si se tiene en cuenta que la ingestión de 10-50 ooquistes esporulados puede ocasionar el fallo reproductivo en la oveja.
Patogenia, signos clínicos y lesiones de la toxoplasmosis en los pequeños rumiantes
- Una vez ingeridos, los ooquistes se desenquistan en el intestino delgado, liberándose los esporozoítos que invaden y se multiplican en las células del intestino y se diferencian en taquizoítos. Los taquizoítos atraviesan la barrera intestinal, se multiplican en los ganglios mesentéricos, originando una hipertrofia ganglionar y en ocasiones, necrosis focal.
- Posteriormente, los taquizoítos se diseminan por la vía linfo-hematógena (días 5-12 post-infección) a otros órganos produciendo focos de inflamación y necrosis. Si el animal está gestante los taquizoítos alcanzan la placenta y se multiplican en los tabiques carunculares maternos del placentoma desde donde invaden las células del trofoblasto fetal y se propagan al resto del feto (toxoplasmosis congénita).
- Con el desarrollo de la respuesta inmunitaria en el hospedador, los taquizoítos se transforman en bradizoítos en el interior de quistes tisulares localizados principalmente en órganos inmunoprivilegiados como el sistema nervioso central y la musculatura. El animal permanecerá infectado de por vida y será seropositivo.
- La toxoplasmosis adquirida es normalmente asintomática, aunque puede observarse un cuadro febril durante la primera semana post-infección.
- Las consecuencias de la toxoplasmosis congénita dependen de la etapa de la gestación en la que ocurre la infección (Figura 2). Si la infección tiene lugar durante el primer tercio de gestación, cuando el sistema inmunitario del feto no está desarrollado, el parásito atraviesa la placenta y produce graves lesiones, ocasionado la muerte fetal y produciéndose normalmente reabsorciones. A partir de los dos meses de vida el feto es capaz de desarrollar una respuesta inmunitaria parcialmente protectora (dependiente de la ontogenia de su sistema inmunitario) y, consecuentemente, la infección a mitad de la gestación puede resultar en la muerte fetal y el aborto o el nacimiento de animales muertos o débiles. Las infecciones durante el último tercio de gestación, cuando el feto es inmunocompetente, dan lugar a la transmisión vertical del parásito, resultando en el nacimiento de corderos débiles o clínicamente normales pero infectados y resistentes a la toxoplasmosis adquirida.
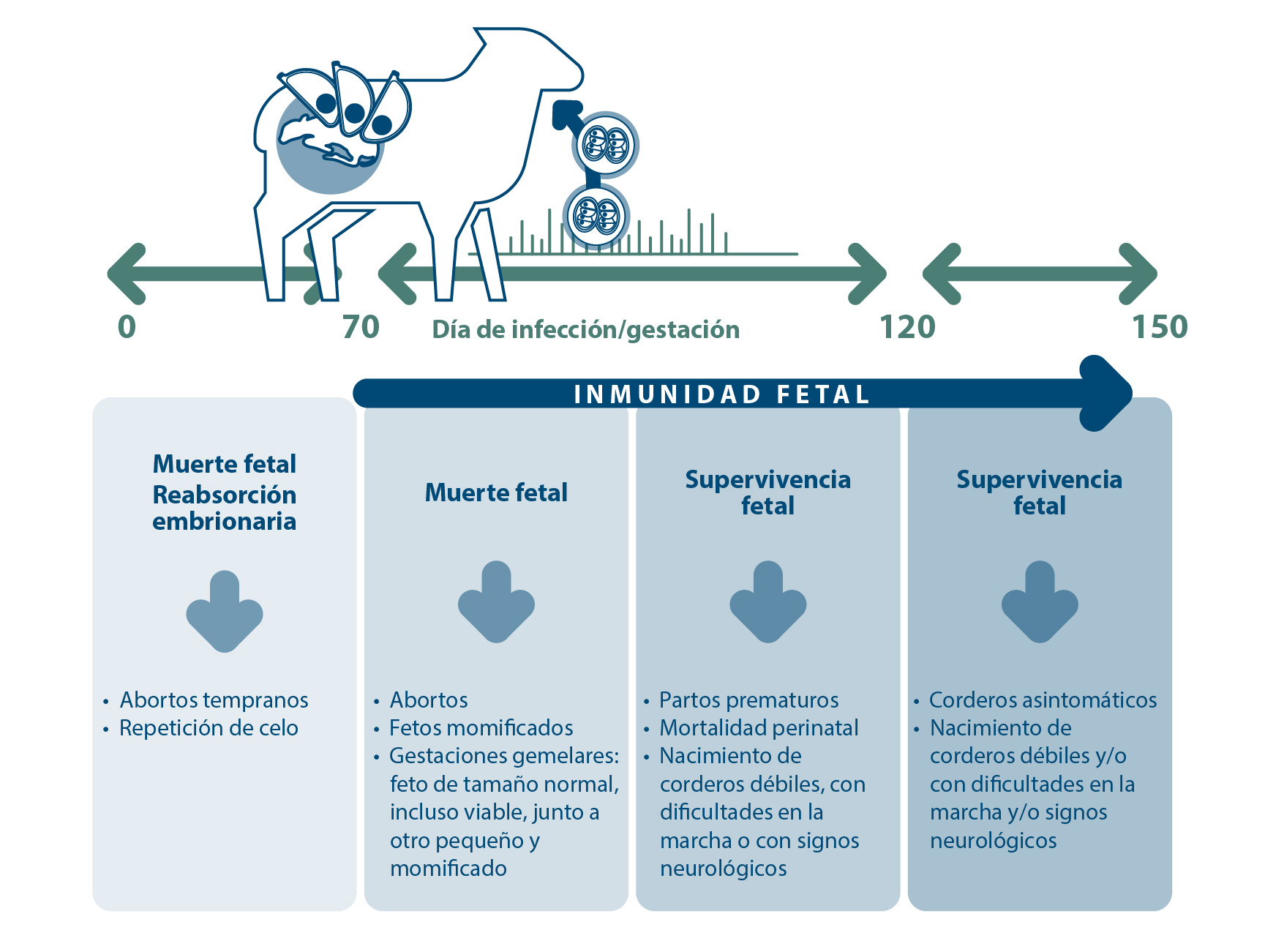
Figura 2. Patogenia y cuadro clínico de la toxoplasmosis congénita.
- En el ganado ovino, la toxoplasmosis congénita ocurre cuando una oveja gestante se infecta por primera vez. Una vez infectada, esta permanece como tal durante toda su vida y la inmunidad que desarrolla es capaz de limitar la transmisión del parásito al feto. Por el contrario, tras la primoinfección en el ganado caprino hay posibilidad de transmisión al feto en gestaciones posteriores.
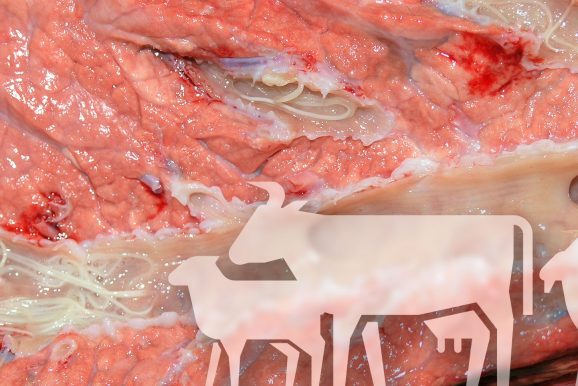
- Clásicamente, el aborto por Toxoplasma se suele observar a partir de las cuatro semanas posteriores a la primoinfección de una oveja gestante y se asocia con la multiplicación del parásito en la placenta y el feto, ocasionando lesiones inflamatorias no supurativas y focos de necrosis, principalmente en el tejido nervioso. Las lesiones placentarias se presentan fundamentalmente en los cotiledones y consisten en focos blanquecinos de necrosis asociados a edema e inflamación (Figura 3).
- En los últimos años, diversas infecciones experimentales realizadas en el ganado ovino han mostrado una nueva presentación clínica de esta enfermedad: el aborto temprano. Éste se caracteriza por ocurrir entre los 7 y 12 días después de la infección y por la ausencia de anticuerpos maternales y del parásito en el feto, ocasionando trombosis en la placenta y leucomalacia en el feto. Hasta el momento no se conoce la patogenia de este tipo de aborto, pero se piensa que podría deberse a un mecanismo inmunomediado.
¿Cómo saber si T. gondii está implicado en casos de aborto en un rebaño?
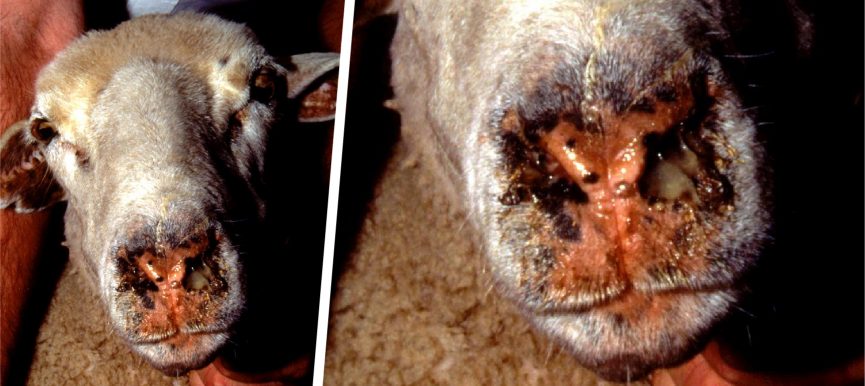
- El diagnóstico clínico-epidemiológico puede ser de utilidad cuando se sospeche de toxoplasmosis. En gestaciones gemelares es muy característico un feto de tamaño normal, incluso viable, junto a otro pequeño y momificado (ver la foto de cabecera). En rebaños seronegativos, los abortos se presentan en forma de brote y hasta 25% (o incluso más) de las ovejas gestantes de cualquier edad pueden abortar. Sin embargo, en rebaños seropositivos los abortos se observan, principalmente, en las ovejas primalas.
- Para confirmar la presencia de la toxoplasmosis en una explotación es necesaria la confirmación laboratorial. Las pruebas serológicas (ej. ELISA) para detectar anticuerpos específicos son solo útiles si se recogen sueros pareados en un intervalo de dos o tres semanas después del aborto para demostrar un aumento en los valores de anticuerpos. Una sola muestra podría ser informativa cuando los títulos son muy elevados. El análisis del feto es determinante para confirmar la presencia de lesiones asociadas a la infección y la presencia del parásito en los órganos diana, como el cerebro o placenta (Figura 3).
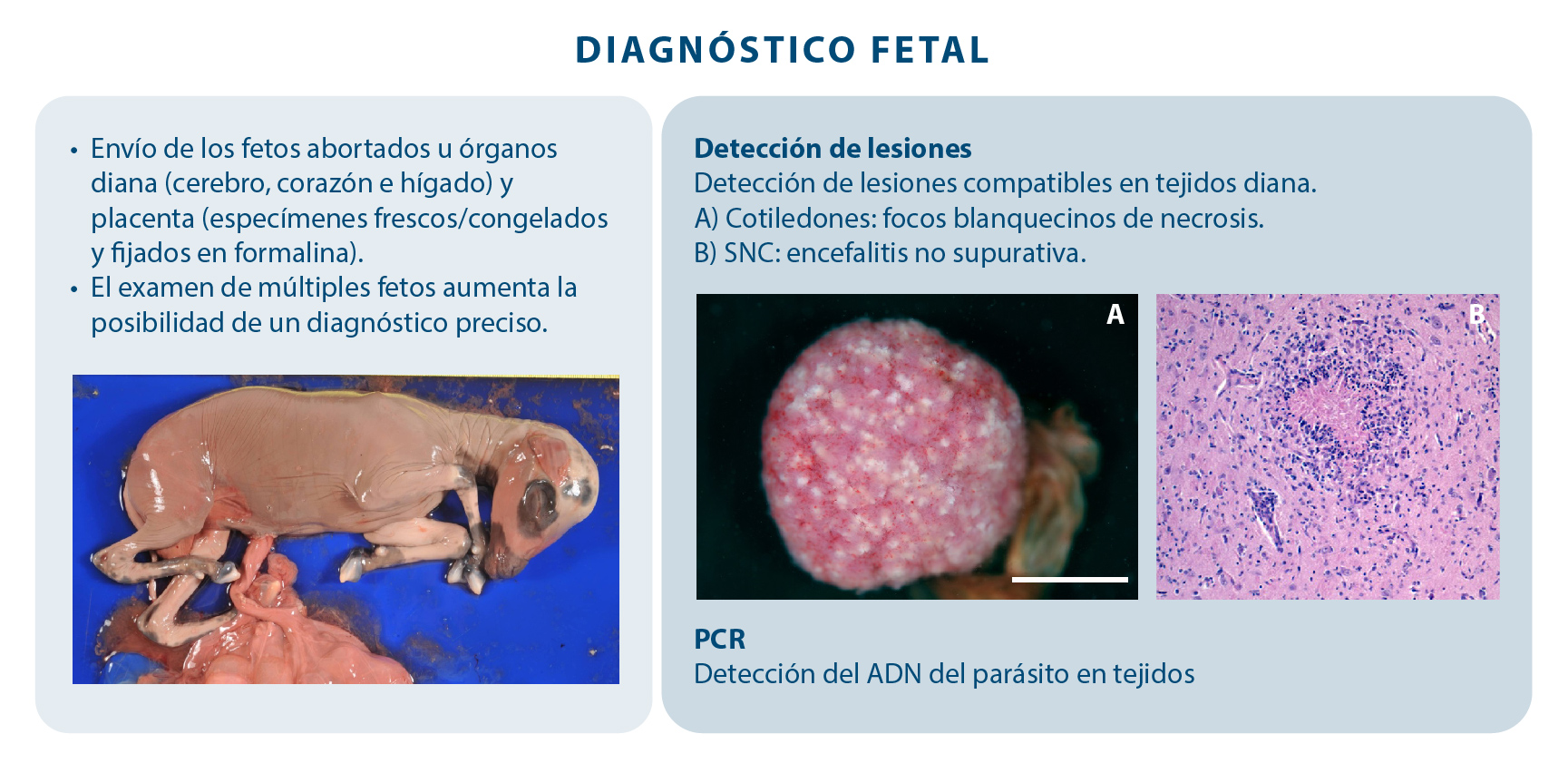
Figura 3. Diagnóstico fetal de la toxoplasmosis ovina.
¿Cómo puedo controlar y prevenir la toxoplasmosis?
- Ante la presentación de un brote, la terapia farmacológica podría ser una opción para el control de la toxoplasmosis ovina. Se podría recomendar la administración de decoquinato (autorizado para su uso solo en el ganado ovino; 2 mg/Kg/día en pienso durante las 14 semanas previas al parto). Ha mostrado cierta utilidad para limitar la infección y se ha observado un aumento de la supervivencia perinatal y del peso de los corderos.
- La vacunación sería la medida más eficaz y económica para controlar esta enfermedad. Existe una vacuna viva atenuada autorizada para su uso en ganado ovino (OVILIS TOXOVAXÒ) y aunque protege frente a la transmisión congénita durante al menos 18 meses, su coste, corta vida útil y la posibilidad de reversión a la virulencia de esta vacuna, dificulta su uso.
- Una vez que un rebaño ha sufrido un cuadro de aborto por toxoplasmosis, se deben mantener en el rebaño las ovejas abortadas ya que no volverán a abortar. En el ganado caprino, esta medida no sería beneficiosa ya que se ha descrito la presencia de abortos en gestaciones posteriores a la primoinfección.
- Asimismo, es importante reforzar las medidas higiénico-sanitarias y de bioseguridad encaminadas a reducir la contaminación ambiental y la transmisión congénita:
- Controlar la población de gatos en la explotación, manteniendo solo gatos adultos.
- Impedir el acceso de los gatos a las zonas de almacenamiento de alimento y agua.
- Retirar abortos y placentas.