El diagnóstico inmunológico es clave en algunas enfermedades parasitarias a la hora de confirmar un diagnóstico clínico presuntivo, evaluar el estado sanitario de un rebaño y diseñar un plan de control o realizar estudios epidemiológicos, dependiendo de la enfermedad parasitaria objeto de estudio y del objetivo de la prueba (pruebas directas o indirectas) (Tablas 1 y 2).
¿Cuál es el fundamento de las pruebas inmunológicas?
En la respuesta inmunitaria que desarrolla el hospedador frente a los patógenos juegan un papel clave los linfocitos T. En primer lugar, las células presentadoras de antígeno (Ag) activan los linfocitos T que se diferencian en linfocitos T efectores o de memoria. Los linfocitos T efectores, a su vez, activan los linfocitos B que inducen la producción específica de anticuerpos (Acs) o inmunolobulinas (Igs) (Figura 1). El reconocimiento de las proteínas (Ags) del patógeno por los linfocitos T o por los Acs (reacción Ag-Ac) sienta las bases del diagnóstico inmunológico.
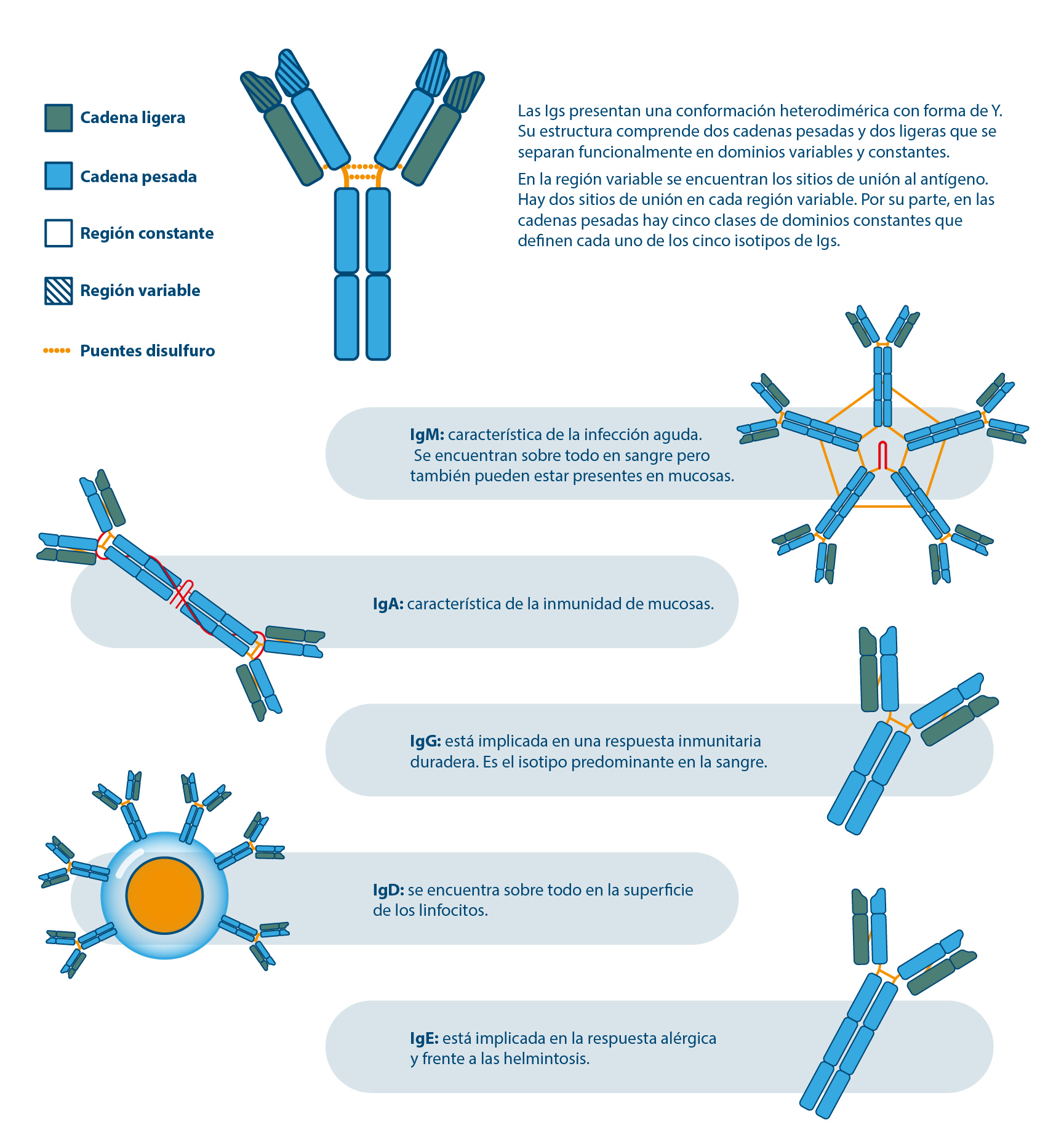
Figura 1. Estructura e isotipos de inmunoglobulinas.
Las pruebas inmunológicas que se emplean habitualmente en el diagnóstico de las enfermedades parasitarias son las que se basan en la reacción Ag-Ac. Por su parte, las pruebas inmunológicas que se basan en la detección de la respuesta inmunitaria de base celular (p. ej. la prueba de intradermorreacción, que se desarrolló para estudiar la respuesta inmunitaria desarrollada por el ganado bovino infectado con Tritrichomonas foetus) no se utilizan en el diagnóstico rutinario y no se tratarán en este artículo.
Las pruebas inmunológicas que se basan en la reacción Ag-Ac se pueden clasificar en dos grandes grupos: i) directas cuyo objetivo es detectar al agente etiológico (p. ej. el patógeno completo o sus proteínas) e ii) indirectas (habitualmente nos referimos a ellas como pruebas serológicas) para detectar los Acs que el hospedador desarrolla tras la exposición al patógeno. La visualización del complejo Ag-Ac puede ser visible a simple vista (p. ej. en la técnica de aglutinación) o invisible (p. ej. la prueba ELISA) para cuya detección se emplean moléculas marcadoras (enzimas, fluorocromos, etc.). Dichas moléculas se unen a los complejos Ag-Ac y amplifican la señal, la cual puede detectarse finalmente a simple vista mediante diferentes tipos de lectores o microscopios.
¿Qué tipo de información ofrece una prueba inmunológica?
Pruebas directas: la detección del agente o de sus proteínas confirma que el animal está infectado en el momento que se realiza la prueba, pero para confirmar el diagnóstico se recomienda asociar el resultado laboratorial al diagnóstico clínico-epidemiológico (p. ej. presencia de signos clínicos o lesiones compatibles con la infección).
Pruebas indirectas: la detección de Acs específicos indica una exposición previa al patógeno. Por tanto, los Acs están presentes tanto en animales con signos clínicos, como en animales que ya han pasado la infección o que permanecen como portadores asintomáticos. Los animales vacunados también desarrollan Acs específicos y, si la vacuna no es marcada, no podremos diferenciar animales vacunados de infectados. Los Acs están presentes y, por tanto, se pueden detectar en diferentes fluidos (p.ej. plasma y suero sanguíneo, líquidos torácico y abdominal, saliva, lágrima, leche). En el caso de los rumiantes las muestras que se analizan con más frecuencia son el suero y la leche.
¿Qué pruebas hay disponibles y cuales se emplean con más frecuencia?
Dentro de las pruebas directas destacan la inmunocromatografía, que es una prueba rápida y sencilla que se realiza en el campo, el ELISA (Enzyme-Linked ImmunoSorbent Assay) sándwich o de captura (Figura 2) y la inmunohistoquímica (IHQ) que requieren de personal y de instrumental especializado (Tabla 1).
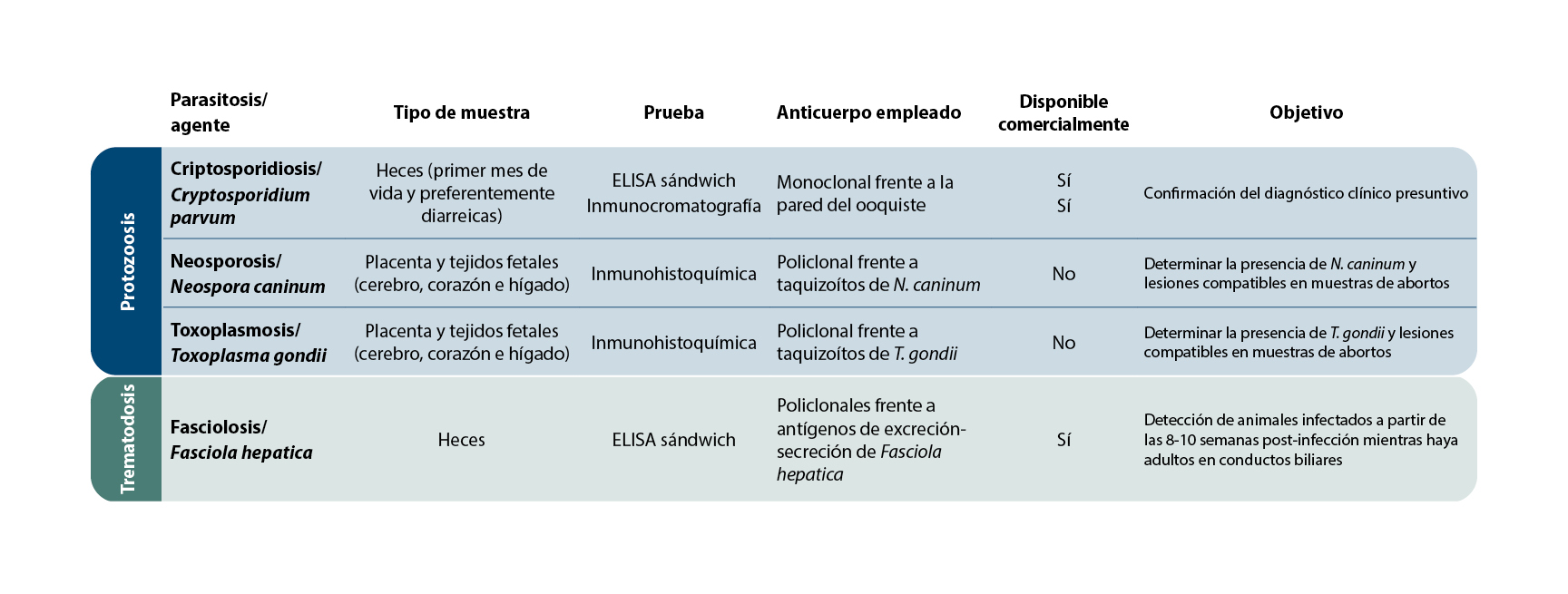
Tabla 1. Pruebas inmunológicas directas que se emplean con más frecuencia.
- Las pruebas rápidas (point of care -POC-) (p. ej. la inmunocromatografía para el diagnóstico de la criptosporidiosis) se basan en la migración de la muestra a través de una membrana de nitrocelulosa durante la cual el Ag presente en la muestra se encontrará con un Ac específico. Los complejos Ag-Ac quedarán inmovilizados cuando se encuentren con un Ac inmovilizado desarrollado frente al Ag y marcado con nanopartículas coloreadas (metales pesados como el oro o el selenio) originándose una reacción colorimétrica en la zona de captura (color rosa o azul). Es una prueba rápida, sencilla y no necesita equipamiento ni personal especializado.
- La prueba ELISA sándwich se basa en la detección del antígeno presente en la muestra mediante el empleo de un Ac específico de captura que tapiza el pocillo de las placas ELISA. Esta unión se pone de manifiesto al emplear otro Ac frente al mismo antígeno conjugado con una enzima (p. ej. peroxidasa de rábano, fosfatasa alcalina) que origina una reacción colorimétrica al añadir su correspondiente sustrato. Es una prueba automatizable y objetiva.
- La IHQ se basa en la detección de antígenos en muestras de tejidos mediante la utilización de: i) Acs marcados con biotina que se unen a la estreptavidina marcada con una enzima responsable de la reacción colorimétrica tras la adición del sustrato; ii) Acs unidos a polímeros como el dextrano que permiten que se puedan unir un mayor número de moléculas de Ac y de enzima amplificando la señal y confiriendo a este sistema una mayor sensibilidad y especificidad.
- Las principales limitaciones de las pruebas directas son: i) suelen ser muy específicas, pero menos sensibles en comparación con las pruebas moleculares (PCR) o el análisis coprológico; ii) la calidad de la muestra está influenciada por la recogida en tiempo y forma y su envío en condiciones adecuadas al laboratorio lo cual repercute en la sensibilidad de la prueba (p. ej. el estado de los tejidos para IHQ); en el caso de las pruebas ELISA e IHQ se requiere de personal y de equipamiento especializado.
- Las muestras indicadas para el empleo de este tipo de técnicas son heces (POC y ELISA sándwich) y tejidos (IHQ).
En cambio, la batería de pruebas indirectas es más amplia incluyendo no solo diferentes pruebas sino también diferentes formatos (Tabla 2).
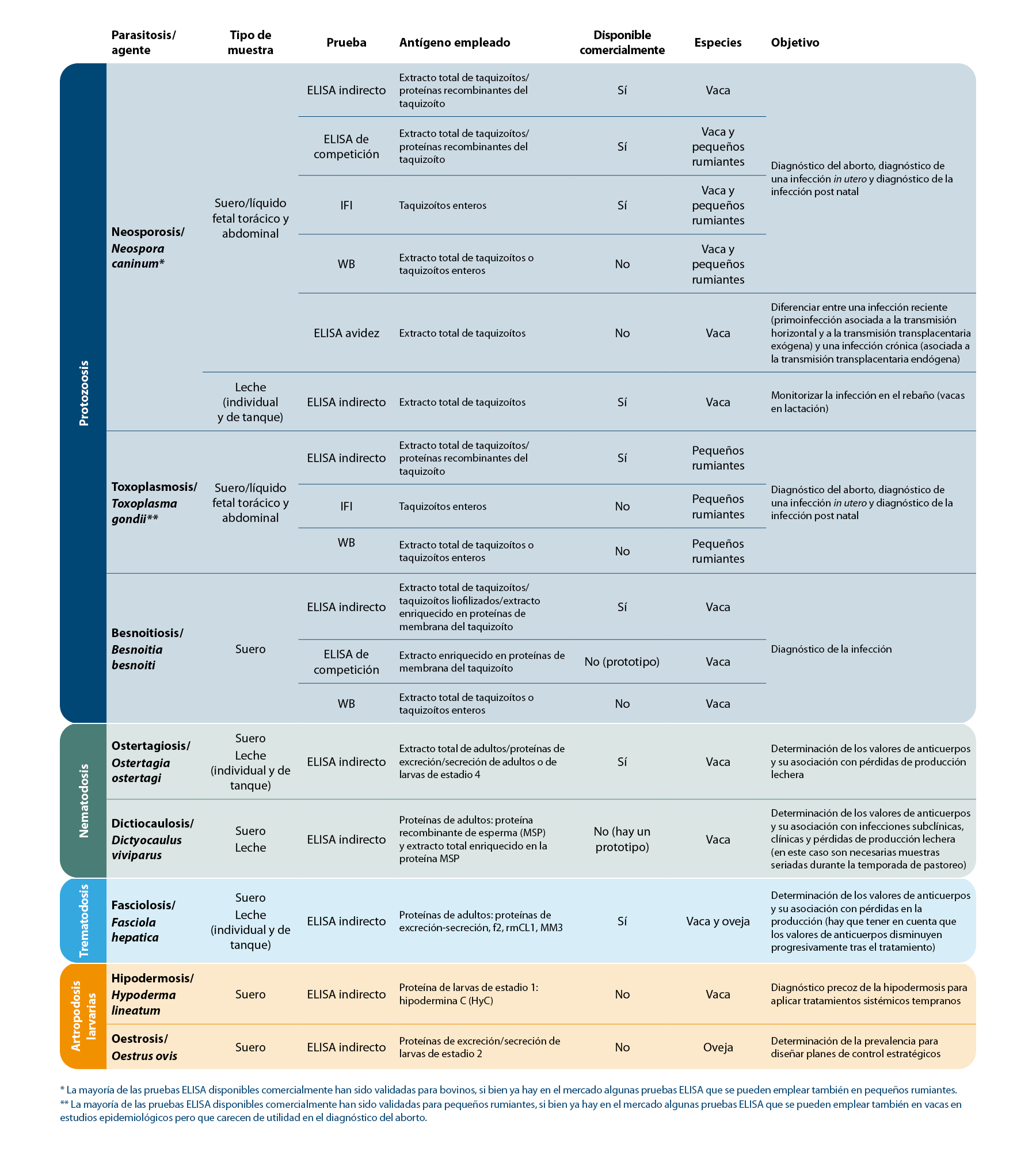
Tabla 2. Pruebas inmunológicas directas que se emplean con más frecuencia.
- La prueba que se emplea con mayor frecuencia y que es la que suele estar disponible comercialmente es la prueba ELISA, destacando dos formatos: el ELISA indirecto y el de competición (Figura 2). La unión Ag-Ac se pone de manifiesto en placas ELISA al emplear un Ac secundario conjugado con una enzima (p. ej. peroxidasa de rábano, fosfatasa alcalina) que da color al añadir su correspondiente sustrato. Se trata de pruebas automatizables y objetivas y requieren de personal y de equipamiento especializado.
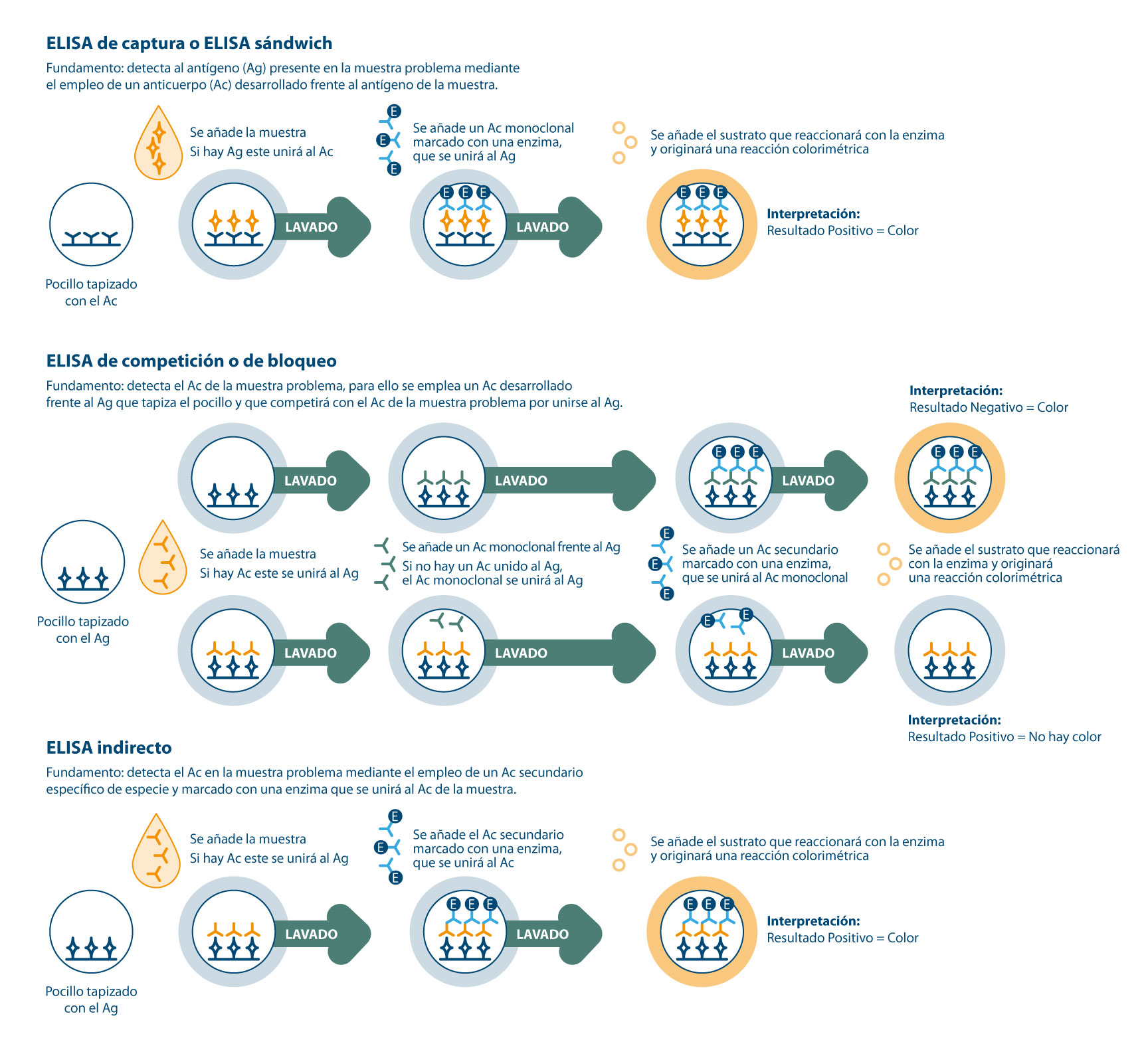
Figura 2. Fundamento de los ELISAs más empleados en el diagnóstico de las enfermedades parasitarias de los rumiantes
- Otras pruebas que se emplean con menor frecuencia no suelen estar disponibles de forma comercial, son desarrolladas y puestas a punto por laboratorios para su utilización y se las conoce habitualmente como pruebas caseras o in house. Estas pruebas que presentan cierto grado de subjetividad dependiente del operario y que se usan, casi exclusivamente, en el diagnóstico de infecciones por los parásitos apicomplejos Toxoplasma, Neospora o Besnoitia son:
- Aglutinación: permite detectar Acs dirigidos frente a proteínas del parásito, formándose macrocomplejos que se visualizarán a simple vista como un punteado. Hay diferentes formatos destacando la microaglutinación que emplea el parásito completo (p. ej. taquizoítos de Toxoplasma) o la aglutinación con partículas de látex que se basa en el empleo de proteínas del parásito unidas a partículas de látex. La ventaja de esta prueba es que no necesita el uso de Acs secundarios por lo que se puede aplicar a cualquier especie animal. Se emplea principalmente en el diagnóstico de la infección en fauna silvestre. Es una prueba subjetiva y que debe validarse para cada una de las especies objeto de estudio. Aunque es una prueba sencilla, sus principales desventajas son la subjetividad en la interpretación de los resultados y la elección del punto de corte.
-
- Inmunofluorescencia indirecta (IFI): permite detectar Acs dirigidos, exclusivamente, frente a proteínas de la superficie del parásito, como por ejemplo el estadio de taquizoíto de Neospora caninum o Toxoplasma gondii. La unión Ag-Ac se pone de manifiesto al emplear un Ac secundario conjugado con fluoresceína, la cual, emite un color verde fluorescente cuando se observa en un microscopio de fluorescencia. Sus principales desventajas son la subjetividad en la interpretación de los resultados, la elección del punto de corte que depende de variables como la dilución del conjugado, la especie y la edad del animal y se necesita experiencia para la interpretación de los resultados.
- El Western blot: es una técnica de diagnóstico que permite detectar Acs específicos frente a las proteínas del parásito que previamente han sido transferidas a una membrana de nitrocelulosa o de fluoruro de polivinilideno (PVDF). Posteriormente, se emplea un Ac secundario conjugado con una enzima que da color al añadir su correspondiente sustrato y las proteínas reconocidas se visualizan como bandas coloreadas en la membrana. Es una prueba altamente sensible y específica. Mientras que la IFI y el ELISA se usan en el diagnóstico habitual, el western blot se emplea como prueba confirmatoria en caso de resultados dudosos. Además, esta prueba se utiliza cada vez con más frecuencia como técnica de referencia en la validación de otras pruebas serológicas. Esta prueba requiere personal e instrumental especializado, es la que requiere más tiempo y se necesita experiencia para la interpretación de los resultados.
- Puntos clave para tener en cuenta en el diagnóstico inmunológico de las enfermedades parasitarias de los rumiantes
- La placenta sindesmocorial de los rumiantes no permite el paso de Igs de la madre al feto. Por tanto, el recién nacido nace agammaglobulinémico y necesita una adecuada transferencia de inmunidad pasiva a través de la toma del calostro materno hasta que su sistema inmunitario madura y comience a sintetizar sus propias Igs a partir de la segunda semana de vida. Este hecho va a influir en el diagnóstico indirecto de una infección in utero (p. ej. por Neospora caninum) en el recién nacido, el cual deberá realizarse previamente a la toma del calostro analizando una muestra de suero precalostral.
- Los valores de Acs calostrales irán descendiendo progresivamente durante los primeros meses de vida. Por tanto, el diagnóstico posnatal o de una infección in utero cuando no ha sido posible el análisis del suero precalostral, se realizará a partir de los 2-3 meses y 6 meses de vida en pequeños rumiantes y ganado vacuno, respectivamente.
- Para poder detectar Acs en un animal parasitado tiene que transcurrir un periodo de tiempo tras la exposición al agente que variará en función del tipo de Ig a detectar:
- La IgM es la primera que se sintetiza durante el desarrollo de una respuesta inmunitaria adaptativa. Por lo general, sus valores aumentan a partir de la primera semana después de la infección y van descendiendo durante las siguientes semanas, si bien en algunas ocasiones pueden persistir valores detectables de IgMs durante meses e incluso años.
- Las primeras IgGs aparecen a partir de las 2-3 semanas después de la infección. Esta Ig está implicada en una respuesta inmunitaria duradera y según se va desarrollando la respuesta de memoria se van generando Acs de alta afinidad (fuerza de unión de un epítopo del Ac con su Ag). La mayoría de las pruebas indirectas (p. ej. ELISAs, inmunofluorescencia, Western blot) se basan en la detección de IgGs. También se han desarrollado ELISAs de avidez que miden la fuerza de unión de los complejos Ag-Ac y que se denomina avidez (fuerza de unión de varios epítopos del Ac con su Ag). Estas pruebas, en el caso del diagnóstico de la infección por Neospora caninum en el ganado bovino, permiten diferenciar una infección reciente (primoinfección asociada a una infección horizontal y a una infección transplacentaria exógena) de una infección crónica (asociada a una infección transplacentaria endógena). En una primoinfección detectaremos Acs de baja avidez y en una infección crónica Acs de alta avidez.
- No hay pruebas que se basen en la detección de IgAs, IgEs e IgDs con utilidad en el diagnóstico de las enfermedades parasitarias de los rumiantes. La IgA, característica de la inmunidad de mucosas, está presente en mucosas de los aparatos respiratorio, digestivo y genitourinario y, al igual que la IgM, se sintetiza de forma temprana. La IgE juega un papel clave en las reacciones alérgicas y en la respuesta inmunitaria protectora frente a las helmintosis. Finalmente, la IgD es la más desconocida y se encuentra sobre todo en la superficie de los linfocitos.
- En algunas enfermedades parasitarias el análisis de muestras pareadas y la detección de la seroconversión o la asociación de seropositividad con los casos clínicos puede confirmar un diagnóstico clínico-epidemiológico presuntivo (p. ej. neosporosis, toxoplasmosis y besnoitiosis). Por el contrario, en otras enfermedades parasitarias el diagnóstico indirecto no tiene utilidad en estos casos (p. ej. helmintosis o piroplasmosis).
- La mayoría de las pruebas están diseñadas y validadas para el análisis de muestras de suero. Sin embargo, en el caso del ganado lechero la muestra de leche ofrece varias ventajas: i) es una muestra menos invasiva; ii) hay una buena correlación entre los resultados obtenidos en muestras pareadas de suero y leche individual; iii) en algunas enfermedades parasitarias el análisis de muestras de tanque de leche permite evaluar el estado sanitario del colectivo de vacas en lactación (p. ej. neosporosis y fasciolosis) e incluso cuantificar posibles pérdidas de la producción lechera asociadas a una infección parasitaria (p. ej. ostertagiosis y fasciolosis) para facilitar la toma de decisiones a la hora de implementar un programa de control basado en el empleo de antihelmínticos (Tabla 2).
- ¿Cuál es la prueba ideal?
- No existe una prueba ideal y en casos de resultados no concluyentes o dudosos habrá que emplear una segunda prueba confirmatoria a posteriori.
- La elección de una prueba debe realizarse en base a los siguientes criterios: elevada sensibilidad y especificidad y, preferiblemente, deberá ser rápida, barata y estar disponible comercialmente y validada para la especie objeto de estudio.

